2926年度の医学群医学類M2解剖学コースが開講しました。ラボセミナーは武井教授が論文紹介を、フロンティア医科学学位プログラム大学院生が研究進捗報告を行いました。
Cell, 2026年(Volume 189, Pages 1802–1819)
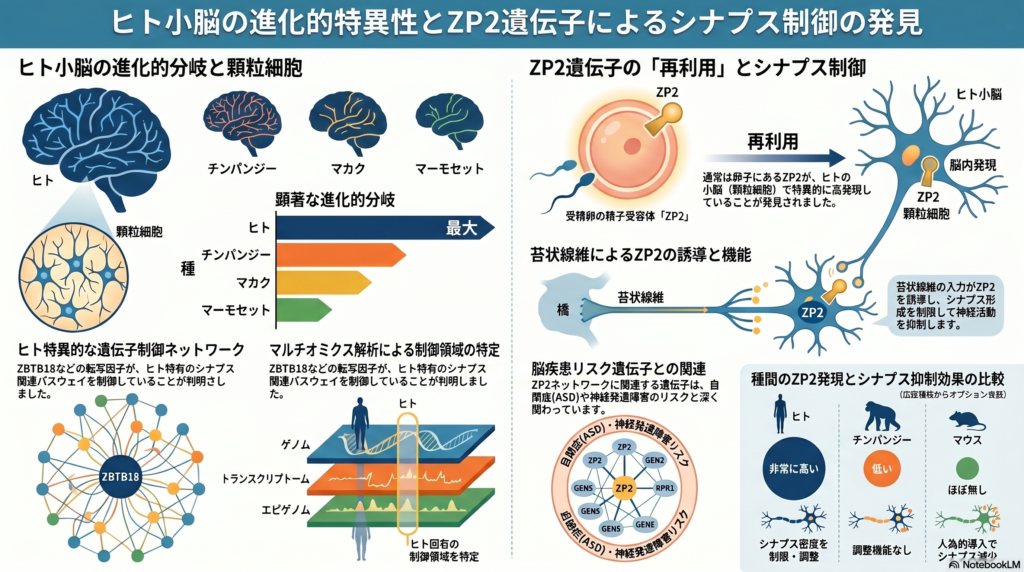
Human-specific features of the cerebellum and ZP2-regulated synapse development ヒト特異的な小脳の特徴とZP2によるシナプス発達制御
Suel-Kee Kim1,19 ∙ Adriana Cherskov1,19 Nenad Sestan1,18,21 et al
Department of Neuroscience, Yale School of Medicine, New Haven, CT, USA
Abstract
本研究は、ヒト小脳が他の霊長類と比べてどのような分子的・細胞学的特徴を持つかを明らかにするため、ヒト、チンパンジー、マカク、マーモセットの成人小脳皮質を対象にsingle-nucleus RNA-seqとsingle-nucleus ATAC-seqを統合したsingle-cell multiome解析を実施した。
その結果、ヒト小脳では特に顆粒細胞(granule cells; GCs)において、シナプス形成や軸索発達に関連する遺伝子群がヒト特異的に変化していた。特に、通常は卵子透明帯で精子受容体として機能するZP2(zona pellucida glycoprotein 2)がヒトGCで高発現していたことが大きな発見であった。
さらにZP2は橋核由来のmossy fiber入力によって誘導され、pontocerebellar glomerulusにおけるシナプス蛋白量を低下させ、神経活動を抑制することが示された。これにより、生殖関連遺伝子がヒト小脳進化においてシナプス制御へ“転用”された可能性が示唆された。
方法
本研究では、ヒト(n=4)、チンパンジー(n=3)、アカゲザル(n=4)、マーモセット(n=4)の成人posterolateral cerebellar cortex(Crus I/IIおよびlobule VI/VII)を用い、single-nucleus RNA sequencing(snRNA-seq)とsingle-nucleus ATAC-seq(snATAC-seq)を統合したsingle-cell multiome解析を実施した。品質管理後、69,302核のRNAデータと63,491核のATACデータを取得し、そのうち60,824核で両データが対応した。UMAPとクラスタリング解析により、granule cell(GC)、Purkinje cell、inhibitory interneuron、astrocyte、Bergmann glia、oligodendrocyte precursor cell(OPC)、oligodendrocyte、microglia、endothelial/pericyteの9主要細胞群を同定した。
種間比較では、DESeq2を用いてヒト特異的・Hominini特異的発現遺伝子を抽出し、GO解析およびSynGO解析により機能的特徴を評価した。さらにSCENIC+を用いて転写因子ネットワークを推定し、ATAC-seqデータからcis-regulatory element(CRE)を解析した。ZP2遺伝子座については447哺乳類ゲノムを用いた比較ゲノム解析を行い、ヒト特異的塩基変異やhuman-gained CREを同定した。
機能解析として、ヒト胎児(PCW18)およびマカク胎仔由来小脳細胞、マウスP1小脳細胞を初代培養し、recombinant human ZP2またはmouse ZP2蛋白を添加した。さらにヒト小脳細胞と橋核細胞のco-cultureを作製し、pontine mossy fiber入力によるZP2誘導を検証した。シナプス形成はSYN1、PSD95、VGAT、GPHNなどの免疫染色で評価し、multi-electrode array(MEA)を用いて神経活動を測定した。加えて、Atoh1-Cre系統を利用したhuman ZP2 knock-in(hZP2-KI)マウスを作製し、in vivoでのシナプス形成、グリア応答、小脳形態を解析した。
Results
single-cell multiome解析により、全霊長類で主要小脳細胞型は保存されていた一方、granule cell(GC)が最も大きな進化的転写変化を示した。ヒトでは744個のupregulated genes、249個のdownregulated genesが同定され、特にsynaptogenesis、synapse organization、local protein translation関連経路が強く変化していた。SCENIC+解析ではZBTB18などの転写因子ネットワークがヒト特異的遺伝子発現と関連していた。
最も注目されたのは、通常は卵子透明帯蛋白として知られるZP2のヒトGC特異的高発現であった。ZP2はヒト小脳で卵巣以上に高発現し、チンパンジー・マカク・マーモセットでは著しく低かった。さらにZP3、ZPBP、ASTLなど生殖関連遺伝子群もヒトGCで協調的に発現していた。ATAC-seq解析ではZP2遺伝子座周辺にヒトGC特異的なchromatin accessibility増加が存在し、human-gained cis-regulatory elementやヒト特異的塩基変異が認められた。特にpromoter領域P2にはATOH1結合を促進しうるヒト特異的E-box motif形成変異が同定された。
発達解析では、ZP2発現は出生後に増加し、glomerular maturation markerであるCDH15やKCND2と並行して上昇した。免疫染色ではZP2がcerebellar glomerulus辺縁部に局在し、中央部のSYN1やPSD95と負相関を示した。PCW18ヒト小脳細胞とpontine細胞のco-cultureでは、pontine mossy fiber入力によってZP2発現が著明に誘導され、同時にSYN1やSYPが低下した。
機能解析では、recombinant human ZP2添加によりヒト・マカク・マウス小脳細胞でSYN1陽性シナプス数が減少した。マウスではVGAT/GPHN陽性 inhibitory synapseも低下した。MEA解析ではZP2処理後にspike firingおよびnetwork burstが有意に減少した。さらにP21 organotypic cerebellar slice cultureやin vivo脳内注入でもシナプス蛋白低下が再現された。
Atoh1-Creを用いたhZP2-KIマウスでは、小脳形態やfoliationに大きな異常はなかったが、GC layer内の興奮性・抑制性シナプスが減少し、IBA1、CD68、S100βも低下した。これらの結果は、ZP2がヒト特異的にpontocerebellar glomerular synapse形成を制御し、神経活動を抑制することを示している。
Discusssion
本研究は、ヒト小脳が単に保存的な脳領域ではなく、特にgranule cell(GC)において強い進化的再構築を受けていることを示した。GO解析ではヒト特異的変化がsynaptogenesis、axon elongation、synapse maturationに集中しており、ヒト小脳進化の中心がシナプス形成制御にあることが示唆された。特に生殖関連遺伝子群が小脳で転用されていた点は極めて特徴的であり、著者らはこれを“evolutionary repurposing”と位置づけている。
ZP2は本来、卵子透明帯で精子結合やpolyspermy防止を担う細胞外マトリックス蛋白である。しかし本研究では、ZP2がヒトGCにおいてpontocerebellar glomerulus周囲へ局在し、シナプス形成を抑制することが示された。著者らは、透明帯におけるZP filament形成と類似した機構が、小脳glomerulus ECMでも働く可能性を提唱している。実際、ZP3やASTLなど関連分子もヒトGCで発現しており、ECM構造変化を介したシナプス調節が示唆された。
ヒトでは小脳、特にposterolateral cerebellumが著明に拡大している。一方でpontine mossy fiber数はGC増加ほど急増しないため、膨大なGCが限られた入力と適切に結合する必要がある。著者らは、ZP2が過剰なpontocerebellar synapse形成を抑制し、回路成熟を遅延させることで、長期間にわたる回路再編成と高精度な結合形成を可能にしたと考察している。この“developmental delay”はヒト脳進化で知られるneoteny(幼形成熟)とも整合的である。ZP2による神経活動低下は、巨大化したヒトGC集団の代謝負荷軽減にも寄与する可能性がある。GCは膨大な数を持つが発火頻度は比較的低く、ZP2によるsynapse suppressionがエネルギー効率化に寄与している可能性が議論された。
これらに加えて、ASD、SCZ、ADHDなど神経精神疾患関連遺伝子がヒト小脳で特異的変化を示したことから、小脳進化と神経疾患感受性との関連も示唆された。特にZP2発現低下はASDやHuntington病、小脳腫瘍で既報があり、今後はヒト小脳organoidや発達モデルを用いたさらなる検証が期待される。
Molecular_Blueprint_of_Human_Cerebellar_Evolution-2





