本日は、医学類学生とフロンティア医科学学位プログラム学生が研究進捗報告をしました。医療科学類学生が論文紹介をしました。久しぶりに、特任研究員もセミナーに参加しました。
Nature Communications, 2025
Neural xenografts contribute to long-term recovery in stroke via molecular graft-host crosstalk
神経異種移植は分子レベルのグラフト‐宿主クロストークを介して脳卒中の長期回復に寄与する
Rebecca Z. Weber, Ruslan Rust
Institute for Regenerative Medicine, University of Zurich, Switzerland
Abstract
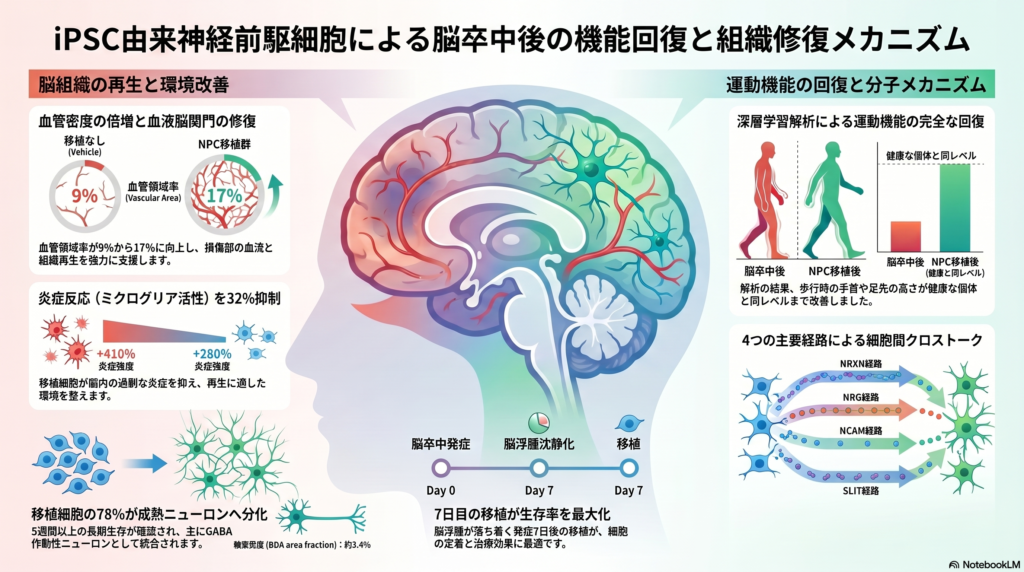
脳卒中は、損傷した神経回路を再生する脳の能力が限られているため、依然として主要な障害原因である。本研究では、iPSC由来の神経前駆細胞(NPC)を局所的に移植することで、脳卒中を受けたマウスにおいて脳修復および長期的な機能回復が改善されることを示した。NPCは5週間以上生存し、主に成熟ニューロンへ分化するとともに、血管新生、血液脳関門の修復、炎症の抑制、神経新生といった再生関連の組織応答に寄与した。NPC治療を受けたマウスでは、ディープラーニングに基づく解析により、歩行および微細運動機能の改善が確認された。単一核RNAシーケンス解析により、移植細胞は主にGABA作動性およびグルタミン酸作動性の表現型をとることが明らかとなり、特にGABA作動性細胞はネurexin、neuregulin、神経細胞接着分子(NCAM)、SLITといったシグナル経路を介して宿主とのクロストークに関与していた。本研究の結果は、神経異種移植がどのように脳卒中後の組織と相互作用し、構造的および機能的修復を促進するのかという機序的理解を提供するものであり、NPC移植が脳卒中後の長期回復を促進する治療法として有望であることを示唆している。
Results
本研究では、iPSC由来NPCを脳卒中後7日に移植したところ、多面的な回復効果が確認された。まず、移植細胞は少なくとも35日以上生存し、初期2週間は安定、その後増加傾向を示した。これは移植細胞が単に残存するだけでなく、増殖や適応を伴う可能性を示唆する。また、梗塞体積はNPC群で2.24 mm³、対照群で3.66 mm³と減少傾向を示したが、有意差には至らなかった(p = 0.09)。
炎症に関しては、ミクログリア活性(Iba1)が32%有意に低下し(p = 0.02)、形態学的にもより分岐した非活性状態に近づいた。一方で、GFAP陽性グリア瘢痕には有意差はなく、炎症抑制は主にミクログリア経由で起こることが示唆された。
神経再生の指標として、NF-Hは虚血境界領域で+48%増加し、NF-Lは虚血コアで+63%増加した。さらに軸索トレーサー解析では、軸索密度が1.83%から3.4%へ有意に増加(p = 0.0055)し、移植細胞が神経ネットワーク再構築を促進することが示された。また、移植細胞由来の神経突起は脳梁や対側皮質へ伸長し、広範な接続形成が確認された。
内因性神経新生については、SVZにおいてEdU+/NeuN+細胞が1.5から20へ有意に増加(p < 0.01)し、移植細胞が宿主の神経新生を促進することが明らかとなった。
血管系では、血管密度(17% vs 9%)、長さ(29 vs 18 mm/mm²)、分岐数(651 vs 326)がいずれも有意に増加し(p < 0.001)、さらに血管漏出はコア領域で改善された(+240% vs +435%)。これは血管新生だけでなく成熟も促進されていることを示す。
細胞分化では、移植NPCの78%がニューロン、10%がアストロサイトに分化し、特にGABA(44%)とグルタミン酸(42%)ニューロンが主要であった。最後に行動解析では、rotarodや歩行解析において有意な運動機能改善が認められ、構造的変化が機能回復に結びついていることが示された。
Discussion
本研究は、NPC移植が脳卒中後回復を促進するメカニズムとして、「単なる細胞置換」ではなく「多面的な再生誘導」を示した点に重要な意義がある。まず、移植細胞は長期間生存し、主にニューロンへ分化するが、その効果は細胞自身の神経回路への組み込みだけでは説明できない。実際には、炎症抑制、血管新生、神経新生など複数の再生プロセスが同時に活性化されていた。
本研究で注目すべきはGABA作動性ニューロンである。脳卒中後にはGABAニューロンが約半減するが、本研究では移植細胞の約44%がGABA型へ分化しており、この欠損補填が回復に寄与する可能性が示された。GABA系は興奮毒性の抑制や神経回路の安定化に関与するため、急性期および慢性期の両方で重要な役割を担うと考えられる。
さらに本研究の最大の新規性は、単一核RNA-seqによってグラフトと宿主の分子クロストークを解明した点である。特にNRXN、NRG、NCAM、SLIT経路が同定され、これらはシナプス形成、軸索誘導、血管修復、炎症制御に関与することが知られている。解析では、GABAニューロンがこれらシグナルの主要な「送信者」として機能することが示され、単なる受動的な細胞ではなく、積極的に組織再生を制御する役割を持つことが明らかになった。
また、血管新生に関してはVEGF単独とは異なり、漏出を伴わない成熟血管形成が促進された点が重要である。これはNPCがより制御された血管再生環境を提供する可能性を示す。加えて、SVZでの神経新生促進は、移植細胞がパラクライン作用を通じて内因性修復機構を活性化することを示唆している。
一方で限界として、免疫不全マウスを用いているため免疫応答の影響が評価されていない点、移植細胞の機能的シナプス統合が直接証明されていない点が挙げられる。また、分子機構の一部はin vitro検証にとどまっている。本研究はNPC移植が「細胞補充+分子シグナルによる環境再構築」という二重の作用を通じて脳卒中回復を促進することを示し、再生医療の新たな設計原理を提示した。


