本日は、M2の神経解剖実習を実施した後、輪読会とラボセミナーを行いました。スタッフは週末の大学院説明会と某学会の総会に参加していたため、イベント盛りだくさんで少々お疲れ気味です。大学院説明会には、多くの学生が参加して下さりありがたいです。若い人とお話しできるのは嬉しいです。
ラボセミナーでは、生物学類2年生が下記の論文紹介をしてくださいました。続いて医学類3年生が研究進捗報告をしました。医学類の学生の方は、研究の経験が深い方なので、イントロダクションが十分に練られていました!
DNA Res. 2022 Jun 25;29(4):dsac019. doi: 10.1093/dnares/dsac019.
Whole-genome sequencing analysis and protocol for RNA interference of the endoparasitoid wasp Asobara japonica (寄生蜂Asobara japonicaの全ゲノム解析およびRNA干渉の手順)
Takumi Kamiyama 1 2, Yuko Shimada-Niwa 2 3, Hiroyuki Tanaka 4, Minami Katayama 1, Takayoshi Kuwabara 5, Hitoha Mori 5, Akari Kunihisa 5, Takehiko Itoh 4, Atsushi Toyoda 6, Ryusuke Niwa 2
Abstract
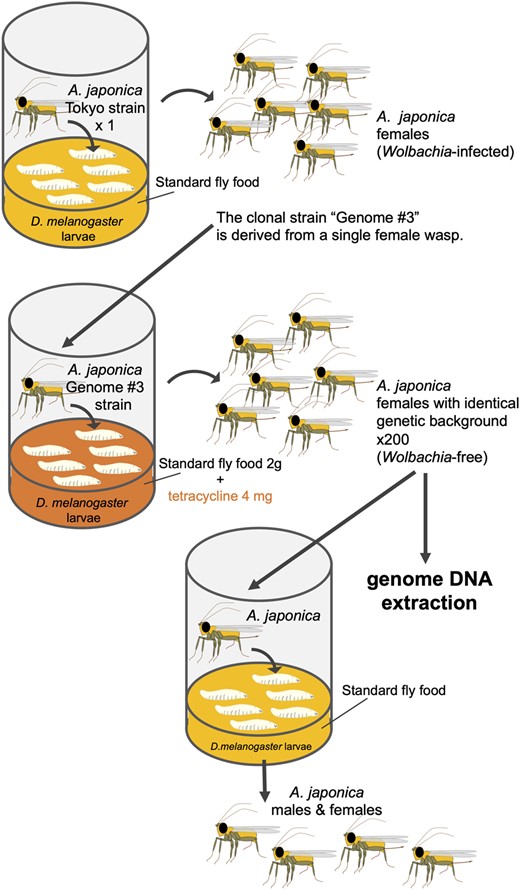
Asobara japonica is an endoparasitic wasp that parasitizes Drosophila flies. It synthesizes various toxic components in the venom gland and injects them into host larvae during oviposition. To identify and characterize these toxic components for enabling parasitism, we performed the whole-genome sequencing (WGS) and devised a protocol for RNA interference (RNAi) with A. japonica. Because it has a parthenogenetic lineage due to Wolbachia infection, we generated a clonal strain from a single wasp to obtain highly homogenous genomic DNA. The WGS analysis revealed that the estimated genome size was 322 Mb with a heterozygosity of 0.132%. We also performed RNA-seq analyses for gene annotation. Based on the qualified WGS platform, we cloned ebony-Aj, which encodes the enzyme N-β-alanyl dopamine synthetase, which is involved in melanin production. The microinjection of double-stranded RNA (dsRNA) targeting ebony-Aj led to body colour changes in adult wasps, phenocopying ebony-Dm mutants. Furthermore, we identified putative venom genes as a target of RNAi, confirming that dsRNA injection-based RNAi specifically suppressed the expression of the target gene in wasp adults. Taken together, our results provide a powerful genetic toolkit for studying the molecular mechanisms of parasitism.
ショウジョウバエに寄生するハチであるショウジョウバエヒメバチ(Asobara japonica)は、毒腺でさまざまな有毒成分を合成し、産卵時に宿主の幼虫に注入する。このハチが寄生を可能にするため、これらの有毒成分を特定し、特性を明らかにするために、私たちはA. japonicaの全ゲノムシーケンス(WGS)を行い、RNA干渉(RNAi)のプロトコルを考案した。A. japonicaはボルバキア感染による単為生殖系統を有しているため、私たちは高度に均質なゲノムDNAを得るために、1匹のハチからクローン系統を生成した。WGS解析により、推定ゲノムサイズは322 Mb、ヘテロ接合度は0.132%であることが明らかになった。また、遺伝子注釈のためにRNA-seq解析も行った。この高品質なWGSプラットフォームを基に、メラニン生成に関与する酵素N-β-アラニルドーパミン合成酵素をコードするebony-Ajをクローニングした。ebony-Ajの標的となる二本鎖RNA(dsRNA)を微量注入したところ、成虫のハチの体色が変化し、ebony-Dm変異体の表現型を再現した。さらに、RNAiの標的となる毒遺伝子候補を特定し、dsRNA注入によるRNAiがハチの成虫において標的遺伝子の発現を特異的に抑制することを確認した。これらの結果を総合すると、私たちの研究結果は寄生の分子メカニズムを研究するための強力な遺伝学的ツールキットを提供する。
Keywords: Asobara japonica; RNA interference; endoparasitoid wasp; parasitism; whole-genome sequencing.
Materials and Methods
Asobara japonicaの全ゲノム解析を実施するため、Illumina HiSeq 2500とPacBio Sequel IIを用いてDNAシーケンスを行った。Illuminaシーケンサーでは、250 bpのリードを持つペアエンドシーケンスを実施し、PacBioシーケンサーではより長いリード長を提供する一分子リアルタイム(SMRT)シーケンスを行った。シーケンスデータのアセンブリには、FALCON-UNZIPソフトウェアを用い、その後、ArrowおよびPilonを使ってデータを修正し、最終的に完全性の高いゲノムを得た。
RNA干渉(RNAi)実験のために、ターゲット遺伝子の二本鎖RNA(dsRNA)を合成し、蛍光緑色タンパク質(GFP)をコントロールに使用した。dsRNAは、ガラスキャピラリーを用いた微細注射器で、宿主ケースから取り出したA. japonica幼虫の腹部に注入した。注入後、ハチは2%寒天プレート上で培養し、RNAi実験には10 µg/µlの濃度でdsRNAを使用した。
毒腺遺伝子の候補を特定するために、RNA-seq解析も実施した。A. japonicaの毒腺サンプルを1日および10日齢の段階で収集し、RNAを抽出、ライブラリ作製後、Illuminaシーケンサーで100 bpのペアエンドリードを生成した。得られたデータを用いて遺伝子発現量を評価し、毒腺で発現する遺伝子候補を特定した。
これらの解析によって、標的遺伝子のノックダウンを確認するため、qRT-PCR(定量リアルタイムPCR)を実施し、各遺伝子発現レベルの相対的変化を評価した。この過程で、トリプレックス実験による平均値を用い、GFP注入群をコントロールとして比較した。
結果
WGS(全ゲノムシーケンス)解析によって、A. japonicaのゲノムサイズは322.2 Mbで、N50値は2.64 Mbとされた。また、ゲノム完全性評価にはBenchmarking Universal Single-Copy Orthologues(BUSCO)を使用し、98.8%の完全BUSCOが確認された。この値は、他の寄生蜂種(例えばミツバチや異なるBraconidae科の寄生蜂)のゲノムデータと同程度の高い完全性を示している。RNA-seq解析では毒腺に特異的に高発現する遺伝子群が同定され、その中でgene003054が有望な毒成分遺伝子として選定された。dsRNAによるRNAi実験でこの遺伝子をノックダウンすると、qRT-PCR結果に基づいて遺伝子発現が大幅に抑制された。また、RNAi効果の特異性を検証するため、他の毒腺遺伝子gene010975の発現を確認したところ、ノックダウン効果はgene003054に限定された。これらの結果から、特定の遺伝子を狙ったRNAiがA. japonicaにおいて実現可能であることが確認された。
議論
本研究により、A. japonicaにおけるRNAi技術が確立され、特異的な毒成分遺伝子の発現を抑制できることが明らかになった。これにより、A. japonicaの寄生メカニズムを分子レベルで解析するための基盤が整ったといえる。寄生蜂の毒成分は農業害虫に特異的に作用する可能性があり、特にショウジョウバエ属の害虫防除に応用できる。このため、A. japonicaの毒成分を利用した生物的防除法の開発が期待される。また、A. japonicaはモデル生物ではないが、Drosophila melanogasterなどの宿主生物の遺伝学的ツールが利用可能であるため、宿主-寄生者の相互作用研究における双方向アプローチが可能となる。本研究は、非モデル生物である寄生蜂を対象としたRNAi技術の開発に貢献し、寄生蜂の進化や宿主免疫回避のメカニズム解明に向けた重要な手がかりを提供する。
限界と応用
dsRNA注入による遺伝子ノックダウンには、正確な注入量の調整が難しい点があり、実験結果の再現性が課題とされる。A. japonicaの毒成分はショウジョウバエ属の害虫に特異的に作用するため、農業害虫の生物的防除への応用が期待されます。また、宿主寄生関係の分子メカニズム研究への利用が見込まれる。




(November 11, 2024)

Les sanglots longs
Des violons
De l’automne
Blessent mon cœur
D’une langueur
Monotone.
Tout suffocant
Et blême, quand
Sonne l’heure,
Je me souviens
Des jours anciens
Et je pleure
Et je m’en vais
Au vent mauvais
Qui m’emporte
Deçà, delà,
Pareil à la
Feuille morte.
— Paul Verlaine, Poèmes saturniens