本日は、医療科学類G30留学生の学生が論文紹介を、医学類M2学生が先週の論文紹介の補足を説明しました。大学院生たちは、講義がスタートしたので忙しそうです。臨床実習の学生たちも学外での実習などで大変忙しそうです。実習前に、スタッフも負けずに邁進したいものです。
Neuroscience Bulletin, 2022年
KIF17 Modulates Epileptic Seizures and Membrane Expression of the NMDA Receptor Subunit NR2B
KIF17はてんかん発作およびNMDA受容体サブユニットNR2Bの膜発現を制御する
Yan Liu, Fei Xiao et al. Department of Neurology, The First Affiliated Hospital of Chongqing Medical University, China
Abstract
Epilepsy is a common and severe brain disease affecting >65 million people worldwide. Recent studies have shown that kinesin superfamily motor protein 17 (KIF17) is expressed in neurons and is involved in regulating the dendrite-targeted transport of N-methyl-D-aspartate receptor subtype 2B (NR2B). However, the effect of KIF17 on epileptic seizures remains to be explored. We found that KIF17 was mainly expressed in neurons and that its expression was increased in epileptic brain tissue. In the kainic acid (KA)-induced epilepsy mouse model, KIF17 overexpression increased the severity of epileptic activity, whereas KIF17 knockdown had the opposite effect. In electrophysiological tests, KIF17 regulated excitatory synaptic transmission, potentially due to KIF17-mediated NR2B membrane expression. In addition, this report provides the first demonstration that KIF17 is modified by SUMOylation (SUMO, small ubiquitin-like modifier), which plays a vital role in the stabilization and maintenance of KIF17 in epilepsy.
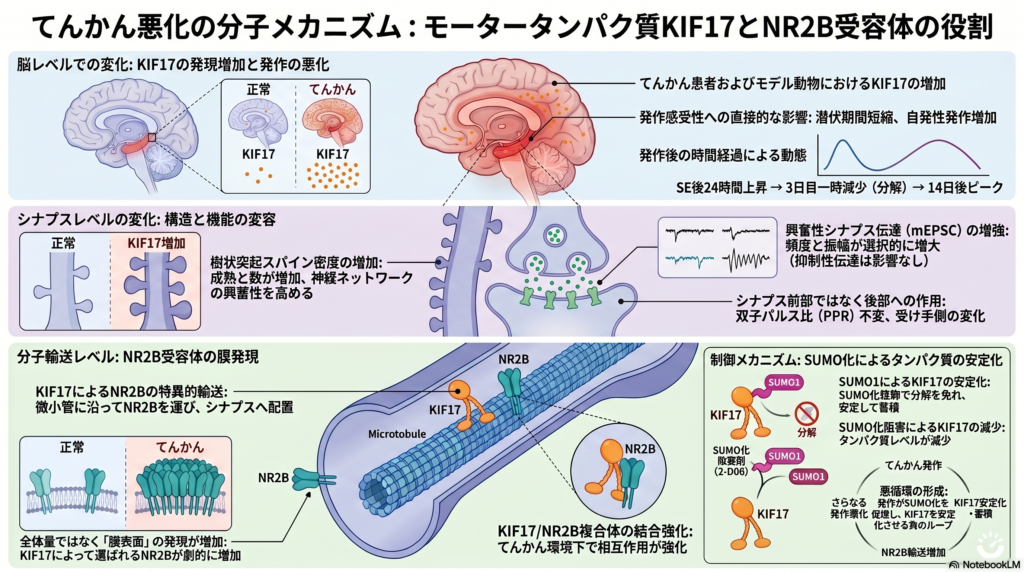
てんかんは、世界で6,500万人以上に影響を及ぼす一般的かつ重篤な脳疾患である。近年の研究により、キネシンスーパーファミリーモータータンパク質17(KIF17)は神経細胞に発現し、N-メチル-D-アスパラギン酸受容体サブタイプ2B(NR2B)の樹状突起への輸送調節に関与していることが示されている。しかし、KIF17がてんかん発作に与える影響についてはこれまで明らかにされていなかった。本研究では、KIF17が主に神経細胞に発現しており、てんかん脳組織においてその発現が増加していることを見出した。カイニン酸(KA)誘発てんかんマウスモデルにおいて、KIF17の過剰発現はてんかん活動の重症度を増加させ、一方でKIF17のノックダウンはこれと逆の効果を示した。電気生理学的解析により、KIF17は興奮性シナプス伝達を調節しており、これはKIF17によるNR2Bの膜発現制御に起因する可能性が示唆された。さらに本研究は、KIF17がSUMO化(SUMO:small ubiquitin-like modifier)による修飾を受けることを初めて示し、この修飾がてんかんにおけるKIF17の安定化および維持に重要な役割を果たすことを明らかにした。
Results
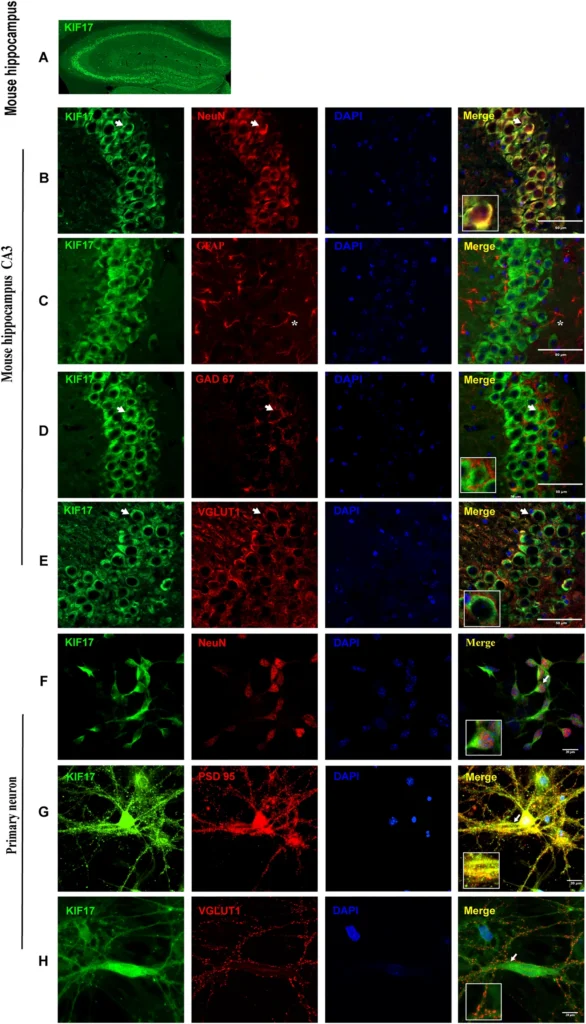
本研究では、KIF17の分布と発現変化を解析し、てんかんにおける役割を検討した。その結果、KIF17は海馬の錐体細胞層および歯状回に強く発現し、主に神経細胞に局在することが示された。またヒト側頭葉てんかん(TLE)患者およびカイニン酸(KA)誘発マウスモデルにおいて、KIF17の発現は有意に増加しており、発作後1日から上昇し14日目にピークに達する動的変化が確認された。機能的解析では、レンチウイルスを用いた操作により、KIF17過剰発現は発作頻度および重症度を増加させ、逆にノックダウンは発作を抑制し潜時を延長させたことから、KIF17が発作活動を促進する因子であることが明らかとなった。
電気生理学的解析では、KIF17は神経興奮性を調節し、特に自発活動電位(sAP)の頻度を増加させることが示された。また、ミニチュア興奮性シナプス後電流(mEPSC)の頻度および振幅はKIF17過剰発現により増加し、ノックダウンにより減少したが、抑制性電流(mIPSC)には変化が認められなかった。さらにペアパルス比(PPR)に変化がないことから、KIF17は主にシナプス後機構を介して興奮性伝達を制御すると考えられる。加えて、KIF17は樹状突起スパイン数を増加させることが確認され、シナプス数の変化がmEPSC頻度の変動に寄与することが示唆された。
分子機構として、KIF17はNMDA受容体サブユニットNR2Bの輸送を制御し、総タンパク量には影響を与えない一方で、膜上のNR2B量を増加させることが明らかとなった。また、免疫沈降解析によりKIF17とNR2Bの結合がてんかん条件下で増強していることが示され、KIF17がNR2Bの膜輸送を促進することが示唆された。さらに、KIF17はSUMO1によるSUMO化修飾を受け、てんかん状態でその修飾が増加していた。SUMO化阻害剤2-D08はKIF17タンパク質量を減少させるがmRNAには影響しないことから、SUMO化はKIF17の安定性維持に寄与すると考えられる。以上より、KIF17はNR2B輸送と興奮性シナプス伝達を介して神経興奮性を増強し、てんかん発作を悪化させる重要な分子であることが示された。
Disucssion
本研究の議論では、KIF17がてんかんの進展に関与する重要な調節因子であることが示されている。KIF17は海馬の錐体細胞層や歯状回といった側頭葉てんかん(TLE)において重要な領域に高発現しており、主に神経細胞のシナプス後部に局在することから、シナプス機能との密接な関連が示唆される。また、ヒトおよびマウスのてんかんモデルでKIF17発現が上昇していたことに加え、過剰発現によって発作が悪化し、ノックダウンで抑制されたことから、KIF17は発作の「原因」というよりも、発作を増強する因子として働く可能性が高いと考えられる。
機能的には、KIF17は抑制性シナプスには影響を与えず、興奮性シナプス伝達のみを選択的に増強することが示された。これは、KIF17がmEPSCの頻度および振幅を変化させる一方でmIPSCには影響しないこと、さらに樹状突起スパイン数を変化させることから、シナプス後機構およびシナプス数の調節を通じて神経興奮性を高めることを意味する。このような興奮性優位の変化は、てんかんの基本病態である興奮/抑制バランスの破綻と一致する。
さらに分子レベルでは、KIF17はNMDA受容体サブユニットNR2Bの輸送を制御し、総タンパク量を変化させずに膜表面への局在を増加させることが明らかとなった。てんかん状態ではKIF17とNR2Bの結合が増加しており、これによりNR2Bのシナプス集積が促進され、結果としてNMDA受容体依存的な興奮性電流が増強されると考えられる。この機構は、神経活動依存的なNR2B輸送の既報とも整合的であり、てんかんにおける過剰興奮の分子基盤を説明するものである。
加えて、本研究はKIF17がSUMO1によるSUMO化修飾を受けることを初めて示し、この修飾がてんかん状態で増加することを明らかにした。SUMO化阻害によりKIF17タンパク質量が減少したことから、SUMO化はKIF17の分解を抑制し安定性を維持する役割を持つと考えられる。したがって、てんかんにおいてはKIF17の発現上昇とSUMO化による安定化が相乗的に働き、NR2B輸送と興奮性シナプス伝達の増強を通じて発作を悪化させると結論づけられる。
KIF17_Mechanisms_in_Epilepsy




