1. シロシビンとは
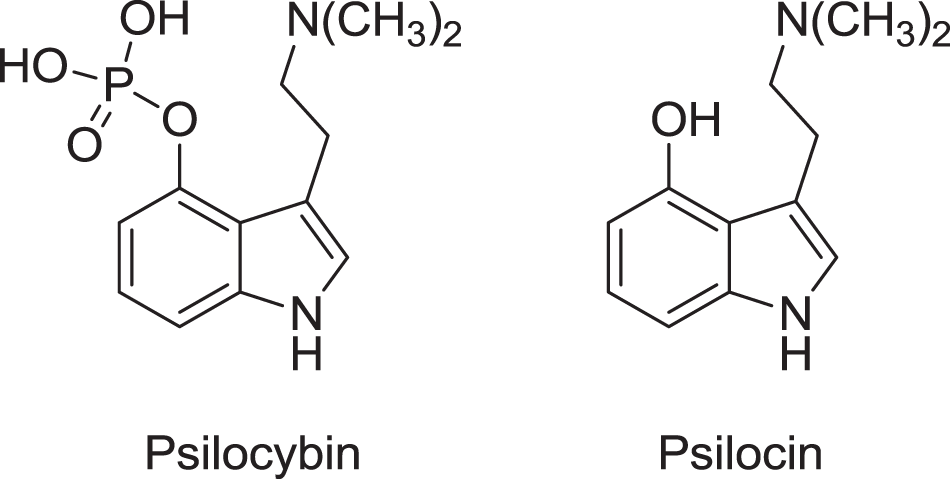
シロシビン(psilocybin)は、マジックマッシュルーム(サイロシベ属など)に含まれる天然の古典的サイケデリクス(幻覚剤)です。体内でシロシン(psilocin)に変換され、主に5-HT₂A受容体アゴニストとして作用します。長年にわたり乱用薬物(Schedule I)に分類されていましたが、2010年代後半から神経科学・精神医学領域で急速に再評価が進んでいます。
2. 作用機序
主な作用機序は以下の通りです。
- デフォルトモードネットワーク(DMN)の抑制:自己参照的反芻思考に関わる脳回路の活動を低下させる
- 神経可塑性の促進:BDNF上昇・シナプス形成促進が動物実験や一部臨床研究で示唆されている
- 感情処理の再編成:扁桃体の過剰反応を和らげ、ネガティブ情動バイアスを修正する可能性がある
- 意識変容体験(mystical experience)との相関:一部研究では、主観的な「神秘体験」の深さが治療効果と相関すると報告されている
3. 臨床エビデンスの現状
3-1. Phase 2 試験(主要な結果)
| 機関・企業 | 対象 | 主な結果 |
| Johns Hopkins大学 | 大うつ病(MDD) | 2回投与で4週後に大幅な症状改善、1年後も効果持続 |
| Imperial College London | 治療抵抗性うつ病(TRD) | SSRIとの直接比較で有意差なし(寛解率は良好) |
| Compass Pathways | TRD | 25 mg単回投与で3週後の症状スコア改善 |
3-2. Phase 3 試験(最新状況:2025〜2026年)
| 企業・製剤 | 主な結果・状況 |
| Compass Pathways / COMP360(合成シロシビン) | Phase 3(COMP005)主要エンドポイント達成。25 mg単回投与 vs プラセボでMADRSスコアが有意に改善(p<0.001、差 -3.6)。2026年末〜2027年初頭のFDA承認申請を目指しローリング申請中。 |
| Cybin / CYB003(重水素化シロシビン誘導体) | Phase 2でMDD患者の75%が4ヶ月後に寛解。FDA Breakthrough Therapy Designation(画期的治療薬指定)取得済み。Phase 3 試験準備中。 |
| Usona Institute(シロシビン) | MDD対象のPhase 3試験進行中。 |
4. 規制上の動向
FDAの動向:FDAは2018年(TRD対象)および2019年(MDD対象)の2つのシロシビン製剤にBreakthrough Therapy Designation(画期的治療薬指定)を付与。この指定により、審査の迅速化・FDAとの密接な協議が可能となっています。
Compass Pathways(COMP360)は2025年11月にFDAとの「ポジティブ」な会合を経て、2026年末〜2027年初頭の承認決定を目指すローリング申請方式を採用。承認されれば世界初の市販シロシビン療法となります。
5. 課題と注意点
| 課題 | 内容 |
| 効果の盲検化困難 | 主観的体験が強く、真のプラセボ対照が難しい |
| 投与様式 | 単回〜2回の投与+専門的な心理サポート(セラピスト同席)が必要 |
| 副作用 | 投与中の不安・混乱・嘔気、稀に恐怖体験(bad trip) |
| 規制・アクセス | 日本では麻薬及び向精神薬取締法でSchedule I相当に指定 |
| 長期安全性 | 大規模・長期データはまだ限定的 |
6. 日本における状況
日本では、シロシビンは麻薬及び向精神薬取締法により麻薬に指定されており、現時点では臨床使用・研究倫理審査を経た試験的使用も非常に限定的です。FDAやEMAの動向が今後の国内規制にも影響を与える可能性があります。
7. まとめ
シロシビンは、現行のSSRI・SNRIでは寛解に至らない治療抵抗性うつ病(TRD)への新たな選択肢として、精神医学・神経科学領域で最も注目される化合物の一つです。単回〜数回投与で数ヶ月に及ぶ持続的な抗うつ効果が示されており、その作用機序には神経可塑性促進やDMN抑制などが関与すると考えられています。2026年〜2027年にかけてFDA承認の可否が焦点となっており、承認されれば精神科薬物療法のパラダイムシフトをもたらす可能性があります。神経免疫との接点(例:サイケデリクスによる神経炎症修飾)も近年研究が進んでおり、今後の展開が注目されます。
参考文献
- Compass Pathways Press Release. Phase 3 COMP005 Primary Endpoint Achievement. 2025.
- Cybin Inc. FDA Breakthrough Therapy Designation for CYB003 in MDD. 2024.
- NIDA. Psychedelic and Dissociative Drugs as Medicines. 2025.
- STAT News. Compass Pathways expects earlier FDA approval decision. November 4, 2025.
- Johns Hopkins Center for Psychedelic and Consciousness Research. https://www.hopkinsmedicine.org/psychiatry/research/psychedelics-research
- Heal DJ et al. Psychedelics: Threshold of a Therapeutic Revolution. Neuropharmacology. 2023.