Cell Resource January 07, 2026
In vivo detection of immune responses via cytokine activity labeling (サイトカイン活性ラベリングによる生体内免疫応答の検出)
Guangqing Lu1 ∙ Shanshan Zhang1 ∙ Mengyang Feng2,3 ∙ Eunha Kim4 ∙ Daniel Cho2,3 ∙ Jae Hyun Kim5 ∙ Hannah Caris2,3 ∙ Lev Silberstein6 ∙ Gloria B. Choi2,3 ∙ Jun R. Huh1
Summary
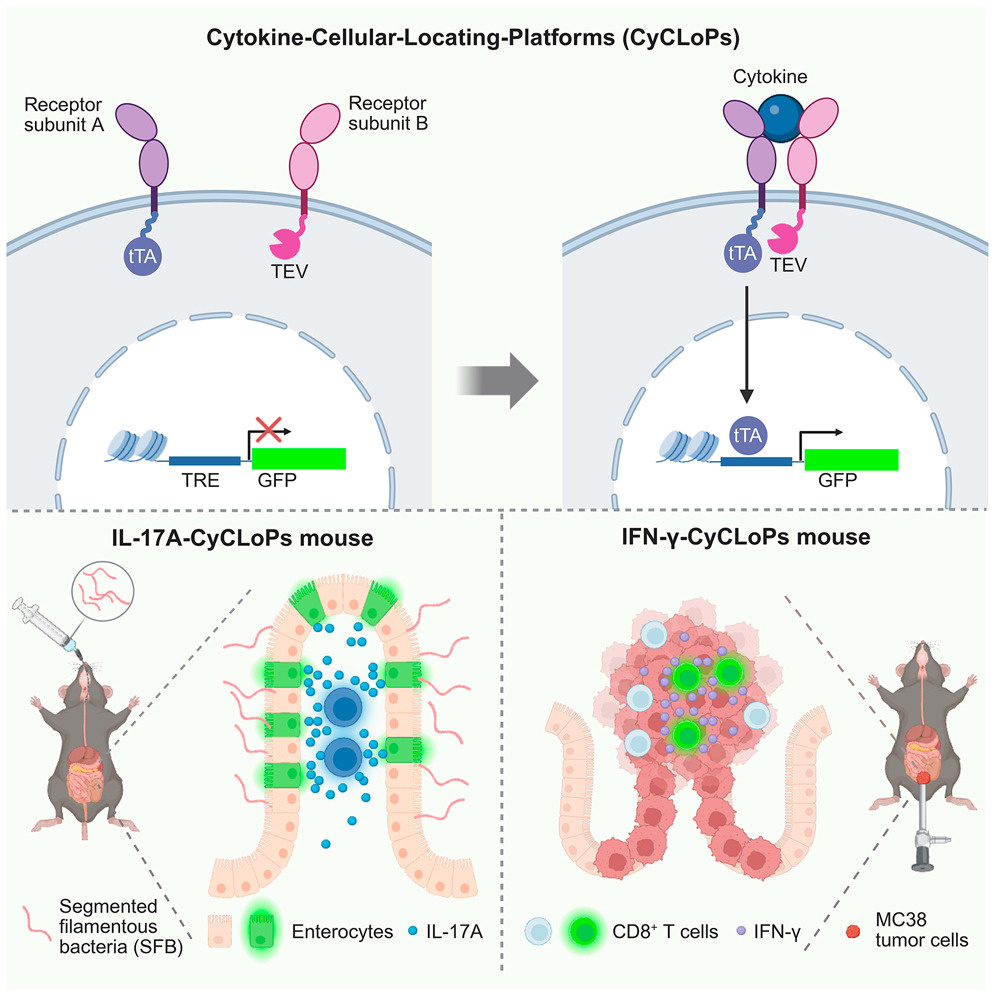
While much is known about the identity and regulation of cytokine-producing cells, the cell types that respond to cytokines remain largely uncharacterized. To address this knowledge gap, we developed “cytokine cellular locating platforms” (CyCLoPs), a reporter system that translates cytokine receptor engagement into a genetically traceable signal. In vitro, CyCLoPs demonstrated high specificity, robust signal-to-background ratios, and broad applicability for probing diverse cytokine receptor interactions. In vivo, interleukin (IL)-17A-CyCLoPs reporter mice enabled the identification of IL-17A-responsive intestinal epithelial cells predominantly localized in the ileal villi following commensal bacterial colonization. Interferon-gamma (IFN-γ)-CyCLoPs reporter mice allowed for the detection of IFN-γ-exposed CD8+ T cells within tumors, which expressed CD36, CD38, and leptin receptor and displayed gene signatures associated with reduced effector function. Collectively, CyCLoPs offers a platform for the direct visualization and characterization of cytokine-induced cellular responses and provides a tool for investigating how cytokines orchestrate distinct immunological outcomes in health and disease.
サイトカインを産生する細胞の種類やその制御機構については多くの知見が蓄積されている一方で、サイトカインに応答する細胞の種類については、いまだ十分に解明されていない。この知識ギャップを埋めるために、本研究では、サイトカイン受容体の結合を遺伝学的に追跡可能なシグナルへと変換するレポーターシステムである「cytokine cellular locating platforms(CyCLoPs)」を開発した。
in vitroにおいて、CyCLoPsは高い特異性、優れたシグナル対バックグラウンド比、ならびに多様なサイトカイン受容体相互作用を解析可能な幅広い汎用性を示した。in vivoでは、IL-17A-CyCLoPsレポーターマウスにより、共生細菌の定着後に回腸絨毛に主として局在するIL-17A応答性腸管上皮細胞を同定することが可能となった。また、IFN-γ-CyCLoPsレポーターマウスを用いることで、腫瘍内に存在するIFN-γに曝露されたCD8⁺T細胞を検出することができ、これらの細胞はCD36、CD38、レプチン受容体を発現し、エフェクター機能の低下に関連する遺伝子シグネチャーを示した。
総じて、CyCLoPsはサイトカインによって誘導される細胞応答を直接可視化・特性解析するためのプラットフォームを提供し、健康および疾患においてサイトカインがいかに異なる免疫学的転帰を制御しているのかを解明するための有用なツールとなる。
Highlights
•Cytokine cellular locating platforms (CyCLoPs) probe cytokine receptor interactions (サイトカイン細胞局在化プラットフォーム(CyCLoPs)は、サイトカイン受容体間相互作用を解析する)
•IL-17A-CyCLoPs detects IL-17A-responsive cells in the ilea upon SFB colonization (IL-17A-CyCLoPsは、SFB定着時に回腸におけるIL-17A応答性細胞を検出する)
•IFN-γ-CyCLoPs facilitates the identification of IFN-γ-exposed CD8+ T cells in tumors (IFN-γ-CyCLoPsは、腫瘍内でIFN-γに曝露されたCD8⁺T細胞の同定を可能にする)
Background
免疫応答はサイトカイン産生細胞の同定を中心に理解されてきたが、実際にどの細胞が、いつ・どこでサイトカインに応答するかを生体内で追跡する手法は乏しかった。サイトカインは受容体複合体形成(多くは二量体化)を介してシグナルを伝達するため、この物理的イベントを転写出力へ変換できれば、応答細胞の同定が可能になる。
Methods
- CyCLoPs設計:受容体サブユニットAにtTA(TEV切断配列付き)、サブユニットBにTEVプロテアーゼを融合。リガンド結合でtTAが切断・核移行し、TetO-H2B-GFPを誘導。
- in vitro検証:NIH-3T3細胞にTRE-EGFPまたは不安定化TRE-d2GFPを導入し、IL-17A/IFN-γなど多数サイトカインで特異性・EC50を評価。
- マウス作製:Rosa26座位にIL-17A-CyCLoPs(IL-17RA-tTA/IL-17RC-TEV)およびIFN-γ-CyCLoPs(IFNγR1-tTA/IFNγR2-TEV)をCRISPR/Cas9でノックイン。UBC-creERT2と交配しタモキシフェン誘導。
- in vivo:サイトカイン投与/中和抗体、SFB定着、MC38腫瘍(皮下・直腸粘膜内)モデル、フローサイトメトリー、免疫染色、RNA-seq。
Results
- 特異性と感度:多くのCyCLoPsで高S/N比。EC50は概ね0.017–1.755 nM。
- IL-17A応答(in vivo):SFB定着後、回腸SI-5〜SI-7でTagBFP⁺IECの20–25%がGFP⁺。GFPは絨毛>陰窩に局在。IL-17A標的遺伝子(例:Cxcl2、Reg3a/b)上昇。
- IFN-γ応答(腫瘍):腫瘍浸潤CD8⁺T細胞でGFP⁺割合が脾臓/mLNより高い。GFP⁺(Tumor_DP)CD8⁺T細胞はGzmd/Prf1/Klrk1低下、CD36・CD38・LEP-R高発現、脂質代謝・血管新生関連遺伝子上昇。
- 依存性検証:IFN-γ中和でCD36/LEP-R発現低下。CD36⁺LEP-R⁺集団はエフェクター機能低下の転写像を再現。
Discussion
CyCLoPsは、サイトカイン受容体相互作用を直接可視化し、応答細胞の空間・機能的同定を可能にする。IL-17Aでは腸上皮の部位特異性、IFN-γでは腫瘍内CD8⁺T細胞の機能低下サブセットを明確化した。将来的に他サイトカイン系へ拡張可能。
Novelty compared to previous studies
- 受容体二量体化→転写出力という一般化可能な設計。
- 生体内での“応答細胞”直接同定(産生細胞ではない)。
- 強度依存的GFPにより応答の量的指標を提供。
Limitations
- 非増殖細胞(例:ニューロン)で感度が低い。
- Rosa26過剰発現・安定H2B-GFPによりリアルタイム性に制限がある。
- 細胞型間比較は同一細胞型内に限定すべきである。
サイクロプス(Cyclops)とは、ギリシャ神話に登場する「一つ目の巨人」を指す言葉で、語源は「円・輪」を意味する kyklos と、「目・顔」を意味する ōps に由来し、「円い目を持つ者」「単眼の存在」という意味を持つ。神話では、雷霆を鍛えた原初の存在や、『オデュッセイア』に登場するポリュペーモスのような怪力の巨人として描かれる。現代では比喩的に、「一点から物事の本質を見抜く存在」や「強力な観測点・センサー」を意味することもあり、本論文のCyCLoPsという名称も、サイトカイン受容体の相互作用という単一の事象を鋭く捉え、可視化する概念を重ねた命名と解釈される。





