NEWS AND VIEWS 10 December 2025
Shared genetic risk in psychiatric disorders 精神疾患における共有された遺伝的リスク
Abdel Abdellaoui
- Abdel Abdellaoui is in the Department of Psychiatry, Amsterdam University Medical Centre, University of Amsterdam, 1105 AZ Amsterdam, the Netherlands.
NatureのNews & Viewsに掲載の本記事は、Grotzingerらの大規模遺伝解析(100万人超の遺伝データ)を受けて、「精神疾患はDSMの診断名ごとに別々の生物学的実体として分かれている」という直感を揺さぶり、むしろ複数の疾患が“同じ遺伝的土台”をかなり共有している可能性を、14疾患横断の枠組みで整理した解説です。
精神疾患は知覚・認知・感情・動機づけといった心の中核機能を損なう一方で、双生児・家系研究から遺伝要因が大きいことは以前から知られていたのに、分子経路や細胞種、神経回路といった生物学的理解が遅れてきました。そこで鍵になるのが「遺伝的構造(genetic architecture)」という考え方で、どんな遺伝変異がどれくらいの頻度で存在し、どの程度の効果量で、どんなパターンでリスクに寄与するのかを束として捉える発想です。
遺伝要因は疾患カスケードの“上流”に位置するため、原因解明の手がかり(分子経路・細胞タイプ・回路)になるだけでなく、環境と遺伝の相互作用を介して「どの発達期(例:幼少期)に」「どんな環境要因(例:トラウマ)が」脆弱性を発症へと転換させるのかを照らす助けにもなる、と記事は述べています。さらに個々の遺伝子機能が未解明でも、多数の変異の効果をまとめたリスクスコアで、脆弱性やレジリエンスのパターンを研究でき、将来的には臨床予測にもつながり得るという立て付けです。データ基盤として強調されるのがPsychiatric Genomics Consortium(PGC)で、オープンサイエンスの枠組みにより国際的にデータを統合し、新しい方法論を適用できる点が進展を支えたと説明されています。
Grotzingerらの中核は、14疾患の間で「共有されるリスク変異がどれほどあるか」を統計的にモデル化し、共有が多いほど“遺伝相関(genetic correlation)が高い”とみなして、疾患同士をクラスタリングしたところ、診断境界をまたいで5つの「ゲノム因子(genomic factors)」にまとまることが見えてきた、という点です(しかもこの5因子で、共通遺伝変異に由来する遺伝率の約3分の2を説明できるとされています)。疾患の内訳は、(1)強迫因子:神経性やせ症(AN)、強迫性障害(OCD)、トゥレット症候群(TS)+不安との一部重なり、(2)統合失調症–双極性障害因子:統合失調症(SCZ)と双極性障害(BD)、(3)神経発達因子:自閉スペクトラム症(ASD)とADHD、(4)内在化因子:大うつ病性障害(MDD)、PTSD、不安障害(AD)、(5)物質使用因子:アルコール使用障害(AUD)、大麻使用障害(CUD)、ニコチン依存(ND)、オピオイド使用障害(OUD)で、ADHDと一部重なる、と整理されています。
ここで重要なのは「単一診断に固有の遺伝変異は少ない」という含意で、DSM分類は臨床的には役立つが、生物学的にはかなり恣意的に見える可能性がある、という問題提起につながります。図(Fig.1)にこの結論を視覚化しており、14疾患(AN, OCD, TS, SCZ, BD, ASD, ADHD, PTSD, MDD, AD, CUD, AUD, ND, OUD)の遺伝相関を並べ、相関が高いほど同じリスク変異を多く共有すること、そしてその相関構造から5つのゲノム因子にまとまることを示しています。また図の凡例では、精神疾患リスクの遺伝シグナルは常に「他の形質に対してマイナス」ではなく、教育達成(EA)、認知能力(COG)、さらにEAに寄与する非認知的スキル(NCOG:動機づけや創造性など)とも多様な相関を示し得ることが明示され、精神疾患に関連する遺伝変異が“価値ある神経多様性(neurodiversity)の源泉”にもなり得る、という視点が提示されています。
さらに記事は、各因子に“生物学的署名”があることを述べ、たとえば統合失調症–双極性障害因子に属する遺伝子が興奮性ニューロンや現実処理に関与する脳領域で高発現であること、神経発達因子が強迫因子や統合失調症–双極性障害因子とも重なることで発達経路の共有を示唆すること、内在化因子ではグリア(神経の支持細胞)に関連する遺伝子が目立ち、気分・不安系は信号を伝えるニューロンそのものより「配線のインフラ」に近いところが効いているかもしれないこと、物質使用因子ではアルコール分解酵素やニコチン受容体のような“物質特異的”シグナルが見られること、加えて物質使用因子は所得や認知など社会経済指標と強く関連し、他因子よりも社会環境経路と絡みやすい可能性があること、そして全因子で胎児期に発現ピークを示す遺伝子が多く早期発達が重要であること、を順に論じます。
これらを踏まえ、精神疾患は「稀な病因変異が決定的に引き起こす」というより、一般集団に広く存在する“よくある”遺伝変異の連続体の端(extremes)で、特定の遺伝の組み合わせとライフイベント・環境ストレスが不利に噛み合ったときに発症しやすい、という連続体モデルが強調され、精神疾患を「欠陥の生物学」とみなすより「自然な変異×環境ストレスの不運な交点」と捉え直すべきだ、というメッセージに結びます。この見方は直ちに倫理・臨床にも波及し、たとえば体外受精に伴う胚スクリーニングで精神疾患の遺伝リスクが高い胚を避ける動きがあるが、もし本研究の因子が“長所と脆弱性の両方を含む正常変異”を反映しているなら、病気リスクと一緒に価値ある神経多様性まで減らしてしまう危険がある、と警鐘を鳴らしています。
一方で本研究の限界として、いまのサンプルサイズは巨大でも、共通変異の全貌を同定するには統計パワーが足りず、著者らの試算では必要規模が現在の数十〜数百倍で、統合失調症で約1,200万人、うつ病で8,000万人超の参加者が必要になると述べられ、診断が比較的稀な精神疾患では“診断ケース集め”だけでその規模に到達するのは現実的でない、とされます。そこで提案されるのが、診断二値(患者/対照)に頼るのではなく、症状・認知・性格・行動などを組み合わせて、基盤となる連続的な遺伝因子をより直接に反映する「量的指標(composite/quantitative measures)」を作り、一般集団コホートを活用して分布全体(臨床の極端例だけでなく)を解析できるようにすることです。
本稿は、精神疾患遺伝学を「診断名の壁の内側」から「共有因子と連続体」へと視点転換させ、診断体系の再考、神経多様性の尊重、そして今後の測定設計(量的表現型の開発)へと議論を押し広げる解説となっています。
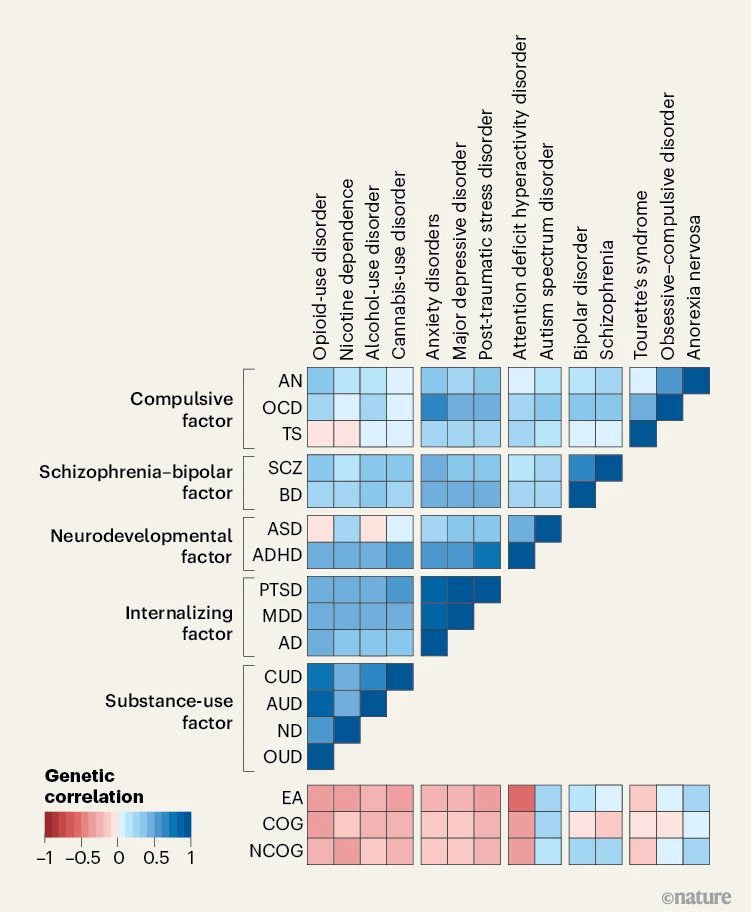
図1. Grotzingerらが解析した14の精神疾患間における遺伝相関(genetic correlation)を体系的に可視化した図であり、「どの疾患同士が、どの程度同じ遺伝的リスク変異を共有しているか」を一目で示しています。図の中央にあるヒートマップでは、神経性やせ症(AN)、強迫性障害(OCD)、トゥレット症候群(TS)、統合失調症(SCZ)、双極性障害(BD)、自閉スペクトラム症(ASD)、注意欠如・多動症(ADHD)、心的外傷後ストレス障害(PTSD)、大うつ病性障害(MDD)、不安障害(AD)、大麻使用障害(CUD)、アルコール使用障害(AUD)、ニコチン依存(ND)、オピオイド使用障害(OUD)の14疾患が縦横に並べられ、各マスの色が2疾患間の遺伝相関の強さを表しています。
凡例に示されているように、青に近いほど正の相関が強く、すなわち「多くの遺伝リスク変異を共有している」ことを意味し、赤に近いほど負の相関、白に近いほど相関が弱いことを示します。この相関構造をもとに、左側には疾患が5つのゲノム因子として括られており、上から順に①強迫因子(Compulsive factor):AN、OCD、TS(および不安との部分的重なり)、②統合失調症–双極性障害因子:SCZとBD、③神経発達因子(Neurodevelopmental factor):ASDとADHD、④内在化因子(Internalizing factor):MDD、PTSD、AD、⑤物質使用因子(Substance-use factor):CUD、AUD、ND、OUD(ADHDと一部重複)と整理されています。
本日は、医療科学類4年生と技術職員、スタッフが協力して動物棟の整理と廃棄物処理を行いました。医学棟内で医学類2年生と久しぶりに会いました。元気そうでした!神経系の試験も頑張ってほしいです。