MITの脳認知科学科准教授のグロリア・チョイの研究室からCell誌に掲載された論文
Cell Article Online nowNovember 25, 2025
IL-1R1-positive dorsal raphe neurons drive self-imposed social withdrawal in sickness (病気のときの自発的な社会的引きこもりは、IL-1R1陽性背側縫線核ニューロンによって駆動される)
Liu Yang 1, Matias L Andina 1, Mario Witkowski 1, Hunter King 2, Ian Wickersham 3, Jun R Huh 4, Gloria B Choi 5
1The Picower Institute for Learning and Memory, Massachusetts Institute of Technology, Cambridge, MA 02139, USA 2Department of Brain and Cognitive Sciences, Massachusetts Institute of Technology, Cambridge, MA 02139, US. 3McGovern Institute for Brain Research, Massachusetts Institute of Technology, Cambridge, MA 02139, USA. 4 Department of Immunology, Blavatnik Institute, Harvard Medical School, Boston, MA 02115, USA 5Bio2Q, Keio University, Tokyo, Japan
Highlights(ハイライト)
- IL-1βは、炎症時に“自発的な社会的引きこもり”を特異的に誘発する
- IL-1R1陽性DRN(背側縫線核)セロトニン作動性ニューロンが、社会的引きこもりを媒介する
- 末梢から中枢へのIL-1βリレーが、持続的な社会的引きこもりを維持する
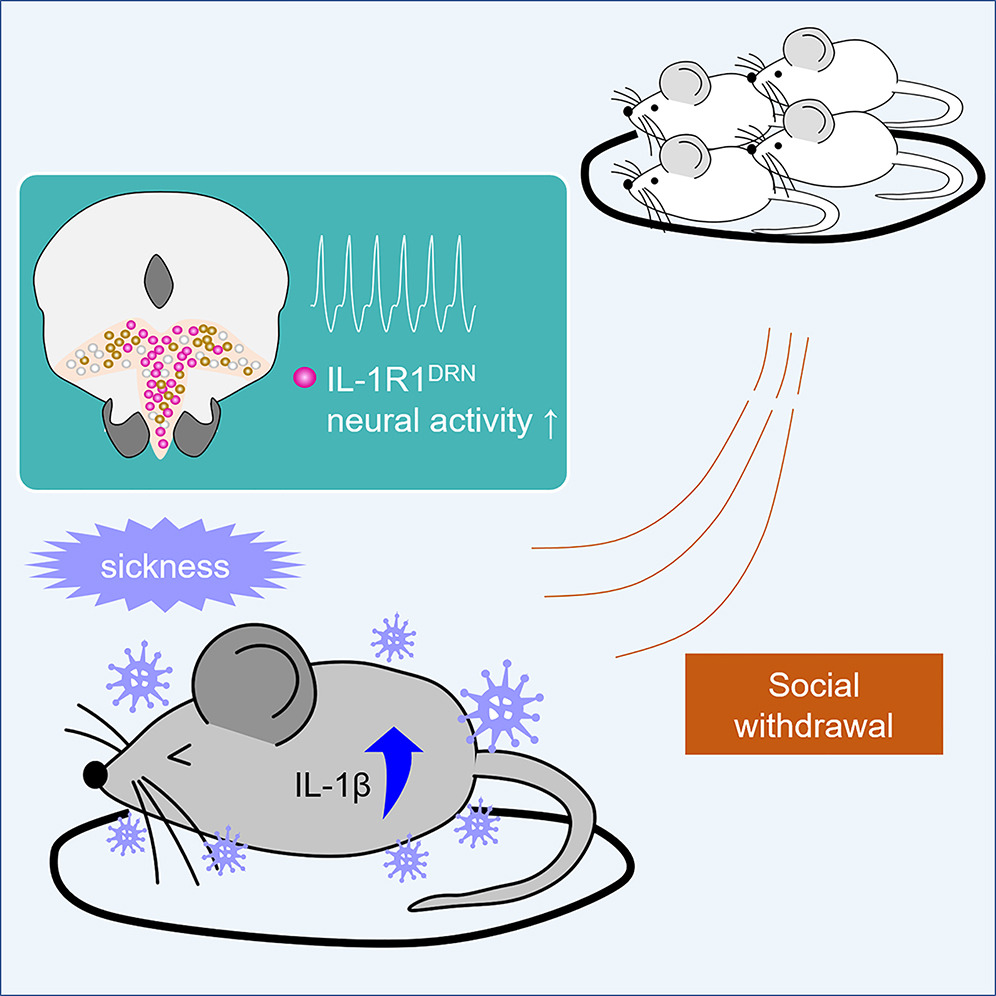
病気の動物は、食欲低下や活動量の低下といった生理的症状にとどまらず、社会的相互作用の低下などの行動変化も示します。病気の際の社会的孤立は、感染拡大を防ぐという進化的な利点をもつことが認識されていますが、その背後にある分子機構および神経機構は明らかになっていません。サイトカインは免疫系由来のシグナル分子であり、炎症時に脳機能に影響を与える神経調節因子として注目されています。本研究では行動スクリーニングを通じて、インターロイキン1β(IL-1β)が病気の状態における社会的引きこもりを促進する、特異な役割を担うことを明らかにしました。IL-1βは、背側縫線核(dorsal raphe nucleus; DRN)においてIL-1R1を発現するニューロン(IL-1R1DRN)の活動を直接修飾します。これらのニューロンを活性化するだけで社会的引きこもりが誘発される一方で、ニューロンの抑制あるいはIL-1R1の遺伝学的欠損によって、全身性炎症時にみられる自発的な社会的孤立は改善されます。我々の知見は、病気の動物において社会的関わりを積極的に断つ行動を促す神経メカニズムを明らかにするものであり、こうした行動適応を駆動する上でIL-1R1^DRNニューロンが重要な役割を果たすことを示しています。
Keywords: LPS; cytokine; dorsal raphe nucleus; infection; interleukin-1; neuroimmunology; pathogen; social behavior.
背景
感染や全身炎症の際、食欲低下や活動性低下に加えて、他者との社会的接触を避ける行動(social withdrawal)が広く観察されます。これは感染拡大を防ぎ、自身の休息を促す「適応的な病気行動」と考えられてきましたが、その分子メカニズムと神経回路はよく分かっていませんでした。
主要な発見
- IL-1β が社会的ひきこもりを特異的に誘導するサイトカインであることを同定 各種炎症性サイトカインを用いたスクリーニングの結果、
- 全身炎症時の「社会的相互作用の低下」は、特に インターロイキン1β(IL-1β) によって強く誘導されることが示されました。
- 背側縫線核(dorsal raphe nucleus, DRN)の IL-1R1 陽性ニューロンが鍵
- IL-1β 受容体 IL-1R1 の発現分布を脳全体で調べた結果、
背側縫線核(DRN)のニューロン群が、社会行動に関わるうえ、髄液中のサイトカインに曝露されやすい位置にあることが分かりました。 - DRN の IL-1R1 陽性ニューロン(多くはセロトニン作動性)が IL-1β に直接応答して活動が上昇し、その人工的な活性化だけで社会的ひきこもり行動が再現されました。
- IL-1β 受容体 IL-1R1 の発現分布を脳全体で調べた結果、
- このニューロン群を抑えると“ひきこもり”だけが消える
- 光遺伝学・遺伝学的操作により、DRN の IL-1R1 陽性ニューロンを抑制したり、これらでの IL-1R1 を欠損させると、
- LPS 投与や IL-1β 投与によって生じる社会的ひきこもりはほぼ消失しましたが、
- 全身倦怠感や活動量低下など、他の病気行動は残存しました。
→ つまり、**「だるいから動けない」副次的現象ではなく、脳内回路による“積極的な自己隔離プログラム”**であることが示されました。
- 光遺伝学・遺伝学的操作により、DRN の IL-1R1 陽性ニューロンを抑制したり、これらでの IL-1R1 を欠損させると、
- DRN から外側中隔(lateral septum)への特定回路が社会行動を制御
- DRN IL-1R1 ニューロンの投射先をトレースしたところ、社会行動に関与すると知られる複数領域に軸索を伸ばしていましたが、
- その中で 中隔の一部(intermediate lateral septum)への投射を光刺激したときのみ, IL-1β 投与時と同様の社会的ひきこもりが誘導されました。
- 末梢炎症から中枢 IL-1β シグナルへの「リレー」が長期のひきこもりを維持
- LPS やサルモネラ感染など、実際の全身炎症モデルでも同じ回路が作動することを確認し、
- 末梢で産生された IL-1β → 中枢 IL-1β → DRN IL-1R1 ニューロンという“リレー”が、持続的な社会的ひきこもりを支えていると結論づけています。
Summary
この知見は、感染時の適応的行動の理解だけでなく、炎症性疾患に伴う社会的ひきこもりや、うつ病・自閉スペクトラム症などの社会行動異常におけるサイトカイン–脳相互作用の関与を考える上でも重要な基盤になると考えられます。
病気のときにひきこもりたくなるのはなぜか?
病気のときに「人に会いたくない」「ひとりでいたい」と感じるのは、単なる気分の問題ではなく、生物学的に組み込まれたプログラムが働いていると考えられています。まず、発熱や免疫応答、組織修復には大量のエネルギーが必要であり、体はそのエネルギーを確保するために、食欲低下や活動量の低下、やる気の低下といった「病気行動(sickness behavior)」を引き起こし、動く・喋る・考えることに使うエネルギーを節約して免疫系に優先的に回そうとします。
さらに、感染症の場合は他者との接触がウイルスや細菌の拡散につながるため、他人に会いたくない、集団から離れたいという方向に行動が変化すると、結果的に仲間への感染拡大を防ぐことができ、集団全体にとって進化的な利益があったと考えられます。このような行動変化の背景には、免疫細胞が放出するIL-1β、TNF、IL-6といったサイトカインの存在があります。これらのサイトカインは血液や脳周囲に達し、脳に「体内で炎症が起きている」という情報を伝えます。
最近の研究では、IL-1βが背側縫線核のIL-1R1陽性セロトニン作動性ニューロンなど特定の神経細胞を直接刺激し、その神経回路が「社会的な関わりを避ける」行動を積極的に駆動していることがマウスで示されています。つまり、「だるいから結果として誰にも会わない」という受動的な現象ではなく、脳の回路レベルで「今はひきこもれ」という命令が出ているイメージです。
加えて、病気や炎症の際には痛みや感覚過敏が強くなり、音や光、人との会話といった刺激が負担になりやすくなります。そのため、脳は刺激の少ない静かな環境を選び、他者との相互作用を減らす方向に行動を誘導し、さらなるストレスや負荷から身を守ろうとします。本来、こうした「ひきこもりモード」は急性期に一時的に働くことで回復と感染拡大防止に役立つ適応的な反応ですが、慢性炎症やストレスが続くとこの回路が長期にわたって過剰に作動し、長引く社会的孤立やうつ様症状につながる可能性も指摘されています。
病気のときにひきこもりたくなるのは、「免疫に専念する」「感染を広げない」「過剰な刺激から身を守る」という目的のために、免疫と脳が連携して私たちの行動を意図的に変えているからだと理解することができます。
