Mol Neurodegener. 2024 Apr 5;19(1):31. doi: 10.1186/s13024-024-00723-x.
An adapted protocol to derive microglia from stem cells and its application in the study of CSF1R-related disorders (幹細胞からミクログリアを誘導するためのプロトコルの改良とCSF1R関連疾患の研究への応用)
Marie-France Dorion # 1 2 3, Diana Casas # 1 3, Irina Shlaifer 2 3, Moein Yaqubi 1 3, Peter Fleming 1 3, Nathan Karpilovsky 3 4, Carol X-Q Chen 2 3, Michael Nicouleau 2 3, Valerio E C Piscopo 2 3, Emma J MacDougall 3 4, Aeshah Alluli 2 3, Taylor M Goldsmith 2 3, Alexandria Schneider 2 3, Samuel Dorion 5, Nathalia Aprahamian 2 3, Adam MacDonald 1 3, Rhalena A Thomas 2 3 4, Roy W R Dudley 6, Jeffrey A Hall 3, Edward A Fon 3 4, Jack P Antel 1 3, Jo Anne Stratton 1 3, Thomas M Durcan 2 3, Roberta La Piana 7, Luke M Healy 8 9
- 1Neuroimmunology Unit, Montreal Neurological Institute-Hospital, McGill University, Montreal, H3A 2B4, Canada.
- 2Early Drug Discovery Unit, Montreal Neurological Institute-Hospital, McGill University, Montreal, H3A 2B4, Canada.

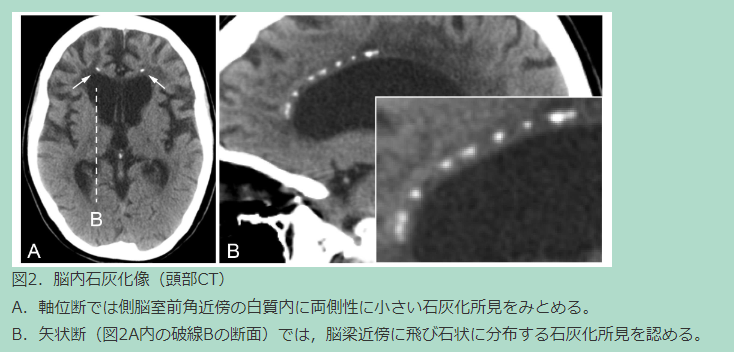
CSF1R遺伝子変異によるALSP/HDLSに関する新たな知見 (新潟大学)
Adult-onset leukoencephalopathy with axonal spheroids and pigmented glia (ALSP)(hereditary diffuse leukoencephalopathy with spheroids (HDLS) とも呼ばれる)は,colony stimulating factor 1 receptor (CSF1R) 遺伝子の変異によって生じる遺伝性白質脳症である。若年性認知症を引き起こしますが,臨床像や病態を含め未解明の部分が多く,有効な治療法がない難病のひとつである。
Abstract
背景
人工多能性幹細胞由来ミクログリア(iMGL)は、健康および疾患におけるミクログリアの機能を研究するための優れたツールである。しかし、iMGLの分化と生存はコロニー刺激因子1受容体(CSF1R)シグナルに大きく依存しているため、iMGLを用いてCSF1Rの病的欠損に伴うミクログリア機能障害を研究することは困難である。
方法
c.2350G>A(p.V784M)のCSF1R変異体を有する成人発症の軸索スフェロイドおよび色素沈着グリアを伴う白質脳症(ALSP: Adult-onset leukoencephalopathy with axonal spheroids and pigmented glia (ALSP)(hereditary diffuse leukoencephalopathy with spheroids (HDLS) とも呼ばれる)患者からミクログリア様細胞の誘導に成功するまで、ミクログリアの分化を促進する成長因子の組み合わせを変更するなど、既存のiMGLプロトコルに連続的な修正を加えた。健康な対照株を用いて、細胞収量評価、ミクログリアマーカー発現の測定、初代ミクログリアとのトランスクリプトーム比較、炎症活性と貪食活性の評価を通して、新しいiMGLプロトコールの品質が検証された。同様に、ALSP患者由来iMGLの分子的および機能的特徴付けを、健常対照iMGLと比較して行った。
結果
新たに考案されたプロトコールにより、培養ヒト初代ミクログリアとの転写産物学的類似性が向上し、高い貪食能と炎症活性を有するiMGLを、オリジナルのプロトコールと比較して~3倍の収量で作製することができた。このプロトコルを用いると、ALSP患者由来のiMGLでは、健常対照者由来のものと比較して、CSF1Rの自己リン酸化と細胞表面発現の減少が観察された。さらに、ALSP患者由来のiMGLは、プリン作動性受容体P2Y12(P2RY12)発現の時間的低下、ミエリン内在化能の亢進、Pam3CSK4に対する炎症反応の亢進を伴う遊走障害を示した。P2RY12発現の低下は、CSF1Rハプロ不全の結果であることが確認された。この特徴は、成熟コントロールのiMGL、およびCSF1RWT/KOとCSF1RWT/E633KのiMGLにおいて、それぞれのアイソジェニックコントロールと比較して、CSF1Rノックダウンまたは阻害後にも観察されたからである。
結論
筆者らは既存のiMGLプロトコールを最適化し、ヒト神経疾患におけるミクログリアの関与を研究する強力なツールを生み出した。最適化されたプロトコールを用いて、我々は初めて、病原性CSF1R変異体を有するALSP患者からiMGLを作製し、予備的な特性解析から、遊走、貪食および炎症活性の機能的変化を指摘した。
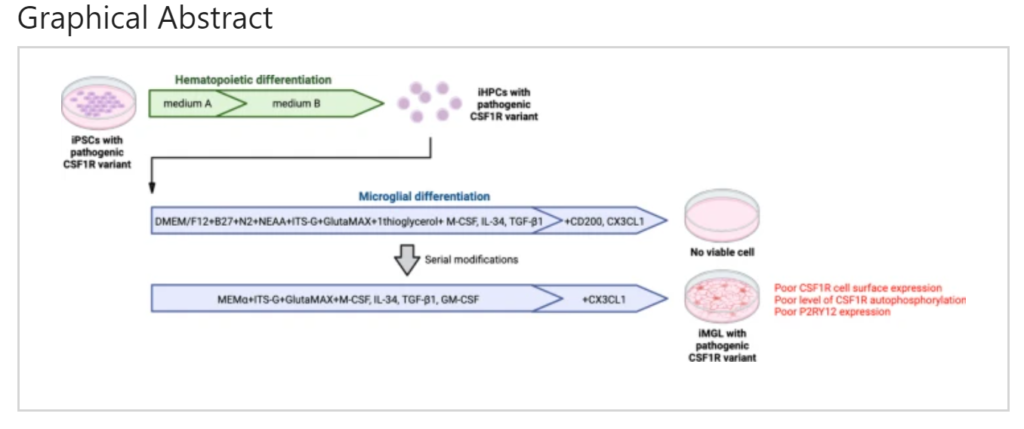
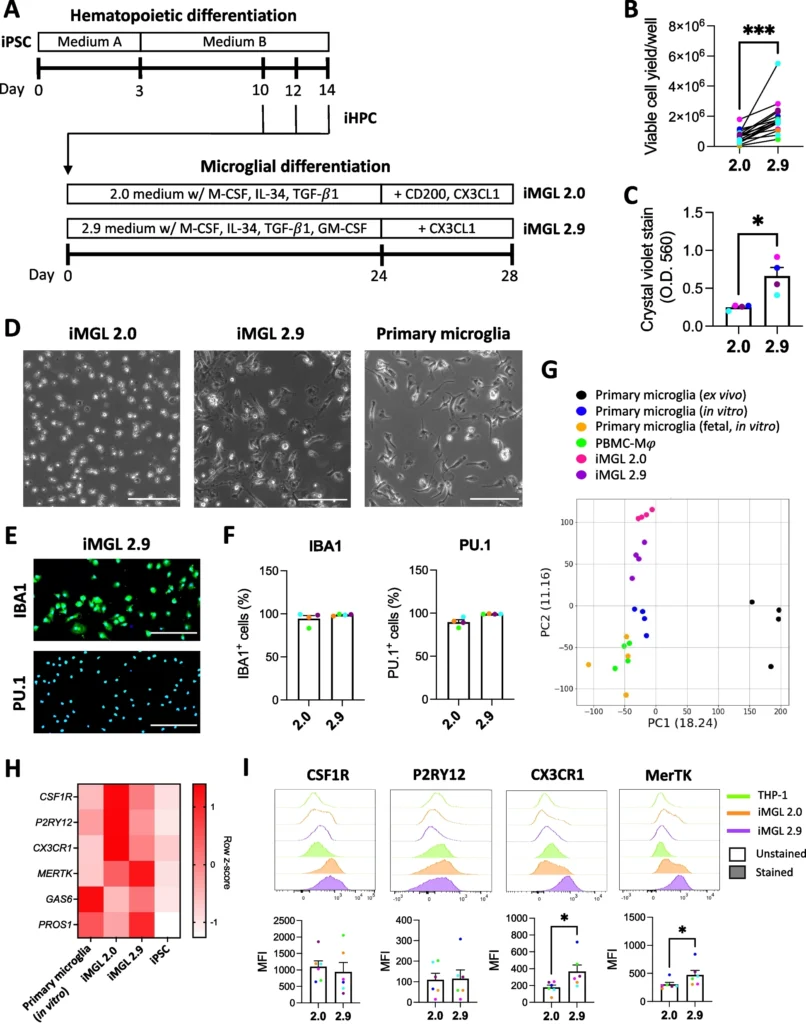
図1.iMGL 2.9の特性: 新しいミクログリア誘導プロトコル「2.9」と従来の「2.0」を比較し、その効果を詳述している。
図1A (プロトコルのスキーマ): 「2.0」と「2.9」プロトコルの違いを図式化しています。特に「2.9」では、成長因子の組み合わせの変更や、その他の培養条件の最適化が施されており、これにより一次ミクログリアに類似した細胞特性が向上しています。
図1B (細胞収率の比較): 新旧プロトコルでのミクログリア様細胞(iMGL)の収率を比較しており、「2.9」プロトコルの方が約3倍の収率改善が見られることを示しています。
図1C (接着試験の結果): crystal violet染色を用いた接着試験の結果を示しており、新プロトコル「2.9」使用時の方がiMGLの接着性が高いことが示されています。
図1D (相差顕微鏡画像): iMGL「2.0」と「2.9」、および一次ミクログリアの顕微鏡画像を比較しています。「2.9」で誘導された細胞は一次ミクログリアに形態が類似していることが分かります。
図1E (免疫染色の画像と定量化): IBA1とPU.1の免疫染色を行った結果の画像と定量データです。「2.9」プロトコルで育成されたiMGLはほぼ100%がこれらのマイクログリアマーカーで陽性であることを示しています。
図1F (IBA1およびPU.1陽性細胞の定量化): 「2.9」プロトコルで誘導されたiMGLはIBA1およびPU.1の発現が高いことが示されています。
図1G (RNAシーケンスによるPCAプロット):「2.0」と「2.9」で誘導されたiMGL、および一次ミクログリアの転写プロファイルをPCAで比較しており、「2.9」が一次ミクログリアにより類似していることが示されています。
図1H (qRT-PCRによるマイクログリアマーカーの表現):「2.9」で誘導されたiMGLは一次ミクログリアと類似のマーカー表現プロファイルを持っていることが示されています。
図1I (フローサイトメトリーによる表面マーカーの分析): CD45およびCX3CR1などの表面マーカーの表現を「2.0」と「2.9」で比較しており、「2.9」の方がこれらのマーカーの表現が高いことが確認されています。
これらの結果から、「2.9」プロトコルは一次ミクログリアに類似した特性を持つミクログリア様細胞の効率的な生成が可能であることが示されており、神経疾患モデルの研究において有用であると考えられます。
議論:
本研究では、誘導多能性幹細胞(iPSC)からミクログリア様細胞(iMGL)を導出するための新しいプロトコルを開発した。この新しいプロトコルは、従来のプロトコルよりも3倍の収率で細胞を生産し、primaryヒトミクログリアとの転写的類似性が向上していることが確認された。特に、ALSP患者由来のiMGLの生成において、新規プロトコルは旧プロトコルと比較して優れた結果を示し、健康な対照群と比較してCSF1Rの自己リン酸化と細胞表面発現が低下することが観察された。これにより、ALSPにおけるミクログリアの機能障害をより詳細に解析する基盤が整った。
新規性:
本研究の新規性は、ALSP患者のiPSCからミクログリア様細胞を効率的に導出するプロトコルを確立した点にある。従来のプロトコルでは、CSF1Rの変異が細胞の分化と生存に重大な影響を与えるため、ALSP患者由来の細胞からミクログリア様細胞を生成することが困難でした。しかし、新しいプロトコルでは、成人発症性白質脳症(ALSP)患者のiPSCからもミクログリア様細胞を高い効率で導出することが可能となり、これにより疾患の分子機構の解明に寄与することが期待される。
限界点:
本研究の限界点としては、新しいプロトコルによって改善されたiMGLの機能が、すべてのCSF1R関連疾患や他の神経疾患モデルにおいて同様の効果を示すかどうかが未検証であることが挙げられる。また、プロトコルの最適化にはさらなる詳細な比較実験が必要であり、特に異なるiPSCライン間での効果の一貫性を確認する必要がある。
潜在的応用:
この新プロトコルは、ALSPのみならず、他の神経疾患におけるミクログリアの研究にも応用可能である。特に、神経炎症や神経変性疾患の病態解明において、疾患特異的なミクログリアの役割を評価する新たなモデルとして有用であると考えられる。さらに、このプロトコルを用いることで、新しい治療薬のスクリーニングや疾患の早期診断方法の開発に貢献する可能性がある。
