Nature Communications volume 5, Article number: 3424 (2014) Published: 06 March 2014
Plexin-A4-dependent retrograde semaphorin 3A signalling regulates the dendritic localization of GluA2-containing AMPA receptors (Plexin-A4依存性の逆行性セマフォリン3AシグナルがGluA2サブユニットを含むAMPA受容体の樹状突起局在を制御している)
Naoya Yamashita, Hiroshi Usui, Fumio Nakamura, Sandy Chen, Yukio Sasaki, Tomonobu Hida, Fumikazu Suto, Masahiko Taniguchi, Kohtaro Takei & Yoshio Goshima
Affiliations
- 1Department of Molecular Pharmacology and Neurobiology, Yokohama City University Graduate School of Medicine, 3-9 Fukuura, Kanazawa-ku, Yokohama 236-0004, Japan.
- 21] Department of Molecular Pharmacology and Neurobiology, Yokohama City University Graduate School of Medicine, 3-9 Fukuura, Kanazawa-ku, Yokohama 236-0004, Japan [2].
- 3National Center of Neurology and Psychiatry, National Institute of Neuroscience, Department of Ultrastructural Research, 4-1-1 Ogawahigashi, Kodaira, Tokyo 187-8502, Japan.
- 4Research Institute for Frontier Medicine, Department of Cell Science, Sapporo Medical University School of Medicine, S-1, W-17, Chuo-ku, Sapporo 060-8556, Japan.
- 51] Department of Molecular Pharmacology and Neurobiology, Yokohama City University Graduate School of Medicine, 3-9 Fukuura, Kanazawa-ku, Yokohama 236-0004, Japan [2] CREST, Japan Science and Technology Agency, 4-1-8 Hontyou, Kawaguchi 332-0012, Japan [3].
- 61] Department of Molecular Pharmacology and Neurobiology, Yokohama City University Graduate School of Medicine, 3-9 Fukuura, Kanazawa-ku, Yokohama 236-0004, Japan [2] CREST, Japan Science and Technology Agency, 4-1-8 Hontyou, Kawaguchi 332-0012, Japan.
Abstract
The dendritic targeting of neurotransmitter receptors is vital for dendritic development and function. However, how such localization is established remains unclear. Here we show that semaphorin 3A (Sema3A) signalling at the axonal growth cone is propagated towards the cell body by retrograde axonal transport and drives AMPA receptor GluA2 to the distal dendrites, which regulates dendritic development. Sema3A enhances glutamate receptor interacting protein 1-dependent localization of GluA2 in dendrites, which is blocked by knockdown of cytoplasmic dynein heavy chain. PlexinA (PlexA), a receptor component for Sema3A, interacts with GluA2 at the immunoglobulin-like Plexin-transcription-factor domain (PlexA-IPT) in somatodendritic regions. Overexpression of PlexA-IPT suppresses dendritic localization of GluA2 and induces aproximal bifurcation phenotype in the apical dendrites of CA1 hippocampal neurons. Thus, we propose a control mechanism by which retrograde Sema3A signalling regulates the glutamate receptor localization through trafficking of cis-interacting PlexA with GluA2 along dendrites.
神経伝達物質受容体の樹状突起への局在は、樹状突起の発達と機能発現に不可欠である。しかし、そのような局在がどのように確立されるかはまだ不明である。我々は、軸索成長円錐部でのセマフォリン3A(Sema3A)シグナルが逆行性軸索輸送によって細胞体に向かって伝播し、AMPA受容体GluA2を樹状突起遠位に駆動し、樹状突起の発達を制御することを明らかにする。Sema3Aは、グルタミン酸受容体相互作用タンパク質1依存的なGluA2の樹状突起への局在を増強するが、これは細胞質ダイニン重鎖のノックダウンにより阻害される。Sema3Aの受容体であるPlexinA(プレキシンA)は、細胞体~樹状突起領域において免疫グロブリン様プレキシン転写因子ドメイン(PlexA-IPT)でGluA2と相互作用していることがわかった。PlexA-IPTを過剰発現させると、GluA2の樹状突起局在が抑制され、CA1海馬ニューロンの尖端樹状突起に尖端部が分岐する表現型が誘導されることを明らかにした。このように、我々は逆行性Sema3Aシグナルが、GluA2とシス相互作用するPlexAを樹状突起に沿って輸送することにより、グルタミン酸受容体の局在を制御する機構を提唱する。
本論文のポイント
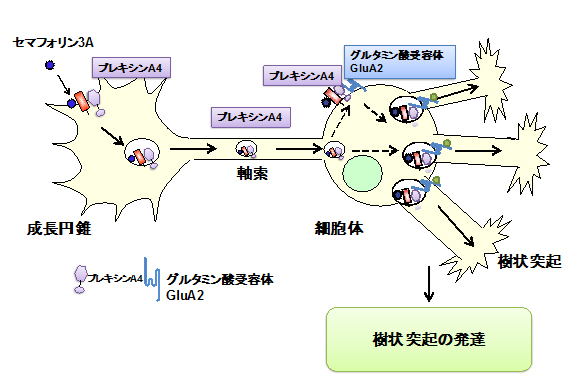
ニューロンは、細胞体、樹状突起、軸索の3つ部分から形成されており、通常、神経を介する情報の伝達は、樹状突起、細胞体、軸索の順序で伝搬していく。今回は、それとは逆の軸索、細胞体、樹状突起という流れの新しい情報の伝達経路を明らかにした。
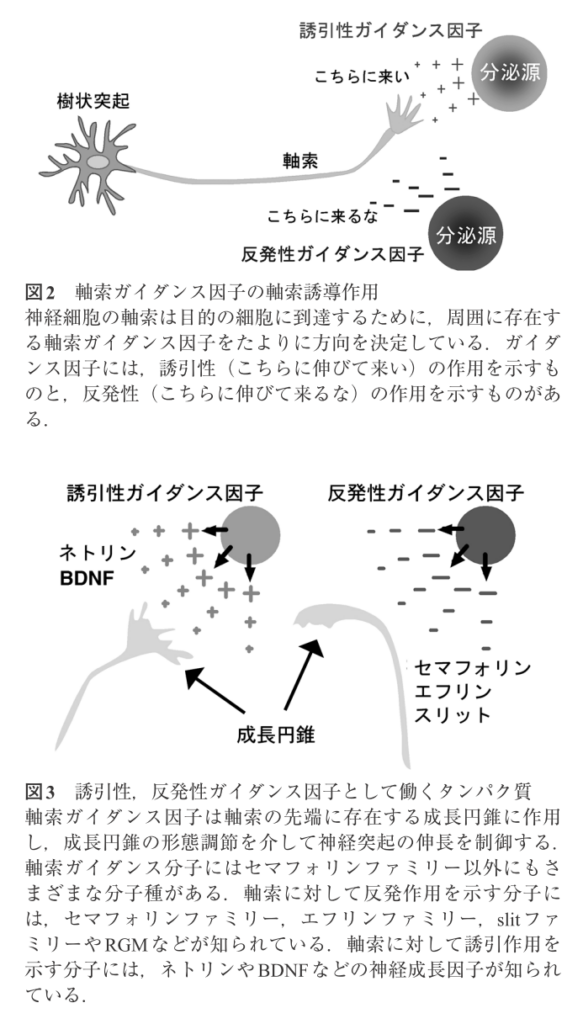
セマフォリン3Aは、軸索が伸びる方向性を制御する分子(軸索誘導因子)として知られていたが、今回、新たに、軸索先端の成長円錐という部位から、逆行性の軸索輸送を介して樹状突起のグルタミン酸受容体の存在する場所を適切にコントロールする仕組みが存在することを明らかにした。
グルタミン酸受容体が正常に働くためには樹状突起の中で正常な場所に存在することが必要で、これが障害されると考えられるアルツハイマー病や統合失調症などの精神神経疾患の新たなメカニズムの解明に繋がる成果といえる。
https://www.yokohama-cu.ac.jp/news/2013/goshima_2014_3.html より抜粋・一部改変
Discussion
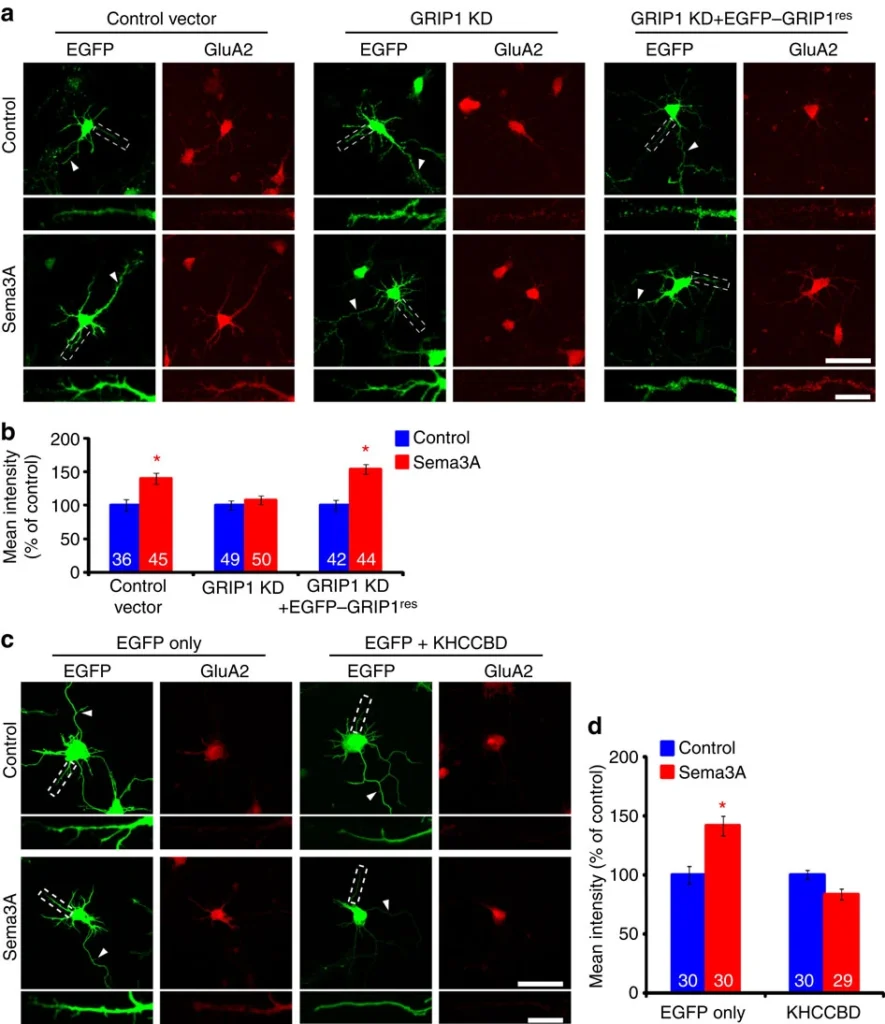
多くの細胞接着分子や細胞外マトリックスタンパク質は、軸索樹状突起の接触部位に局所的に影響を与えることで、分岐やシナプスの形成に関与している。この局所的な事象に加え、一部の神経細胞では軸索が目標に到達するまで樹状突起の発達が遅れることが以前報告されている。このことから、樹状突起の形成には、軸索末端から細胞体へ伝わる逆行性シグナルが必要であることが示唆された。私たちは、海馬の神経細胞において、PlexA4が軸索成長円錐からの逆行性Sema3Aシグナルを仲介し、樹状突起-細胞体領域でGluA2とシス相互作用する受容体として働き、GluA2を樹状突起遠位に運搬することを明らかにした。このように、AMPA受容体の局在を逆行性軸索輸送によって制御する新しいモデルを提案し、軸索誘導分子の多様な生理的役割を明らかにした。
PlexA1-IPTを発現する神経細胞では、sema3A欠損マウスと同様に、樹状突起先端でのGluA2局在の欠損が見られた。さらに、GluA2のノックダウンによりin vitroでのSema3Aによる樹状突起分岐が減弱すること、PlexA-IPTの過剰発現によりin vivoで近位分岐の表現型が生じることを見出した。このように、Sema3Aが樹状突起のパターニングを制御するためには、GluA2とPlexA4の相互作用が必須であることがわかった。GluA2 は、樹状突起の形成に重要な役割を果たすことが示されている。GluA1ではなくGluA2が直接相互作用によってN-カドヘリンをリクルートすることによって樹状突起の発生を制御している。ショウジョウバエのN-カドヘリンは、樹状突起の適切な微細化に必須である。したがって、樹状突起遠位部におけるGluA2の密度が低下すると、N-cadherinが制御する樹状突起の発達が弱まり、分岐の表現型が生じる可能性がある。以上のことから、Sema3AはGluA2の樹状突起局在を制御することで、海馬錐体細胞の樹状突起発達を制御する役割を担っていることが明らかとなった。
以上のことから、遠位軸索に作用するSema3Aが、ダイニンおよびPlexA4依存的な逆行性シグナルを介して、GluA2の局在と樹状突起の発達を制御するというモデルを提唱した。また、PlexA は Sema3A のシグナル伝達受容体としてだけでなく、AMPA 受容体の局在を制御する新たな制御因子として機能する可能性がある。
薬理学 五嶋教授ら研究グループが神経回路形成の新たなメカニズムを解明 !~神経再生や認知症の克服に向けて~
本日は、医学類3年のWさんがAREでの活動報告を行いました。報告会では優秀賞を受賞しました!約10か月間お疲れ様でした。
20230206progressseminar