ACS Nano Article February 18, 2025
Nanoscale Resolution Imaging of Whole Mouse Embryos Using Expansion Microscopy (拡張顕微鏡を用いたマウス胎児全体のナノスケール分解能イメージング)
Jueun Sim 1, Chan E Park 1, In Cho 1, Kyeongbae Min 2, Minho Eom 3, Seungjae Han 3, Hyungju Jeon 4, Eun-Seo Cho 3, Yunjeong Lee 5, Young Hyun Yun 6, Sungho Lee 7, Deok-Hyeon Cheon 6, Jihyun Kim 4 8, Museong Kim 9, Hyun-Ju Cho 10, Ji-Won Park 11, Ajeet Kumar 9, Yosep Chong 12, Jeong Seuk Kang 13, Kiryl D Piatkevich 14 15 16, Erica E Jung 17, Du-Seock Kang 18, Seok-Kyu Kwon 4 19, Jinhyun Kim 4 8 20, Ki-Jun Yoon 9, Jeong-Soo Lee 10 21, Cheol-Hee Kim 11, Myunghwan Choi 7, Jin Woo Kim 9, Mi-Ryoung Song 5, Hyung Jin Choi 6 22, Edward S Boyden 23 24 25, Young-Gyu Yoon 3 26, Jae-Byum Chang 1 9 27
Department of Materials Science and Engineering, Korea Advanced Institute of Science and Technology, Daejeon 34141, Republic of Korea.

膨張顕微鏡法(expansion microscopy)と名付けられたこの手法では、おむつの吸収体としておなじみの材料を利用して生物組織を物理的に膨張させる。マサチューセッツ工科大学(MIT;米国ケンブリッジ)の神経工学者Edward Boydenは、2014年12月に米国立衛生研究所(NIH;メリーランド州ベセスダ)で開かれたシンポジウムで、MITの同僚Fei ChenおよびPaul Tillbergとともに開発したこの技術について発表を行った(訳註:この成果はScience 2015年1月30日号に掲載された。Chen F., Tillberg P. W. & Boyden E. S. Science 347 543-548 (2015))。
要約
脊椎動物の全体をナノスケールで画像化することは、ヒトの疾患を系統的に理解するために不可欠であるが、この目標はまだ達成されていない。拡張顕微鏡法(ExM)は、この目的を達成するための魅力的な選択肢であるが、石灰化した組織の拡張が困難であるため、成体マウスよりも石灰化した身体部位が少ない中期および後期発生段階のマウス胚でさえも拡張できることがまだ実証されていない。ここでは、周期的なdigestionを利用する最先端のExM技術である「Whole-body ExM」を紹介します。この技術は、マウス胚や新生児を4倍に拡大し、解剖学的構造、タンパク質、内在性蛍光タンパク質(FP)の超解像度、立体イメージングを可能にします。Whole-body ExMの主な特徴は、2種類の酵素組成物を交互に複数回適用することです。この消化プロセスを単純に繰り返し、サイクル数を増やすことで、E18.5までのさまざまな段階のマウス胚、さらには胚と比較して石灰化組織の含有量が劇的に異なる新生児マウスも、手間のかかる最適化をすることなく拡張することができます。さらに、全身ExMはFPシグナルを保持する能力があるため、遺伝子組み換えマウスのさまざまな神経構造を可視化することができます。全身ExMは、さまざまな脊椎動物の分子変化の研究を促進する可能性があります。
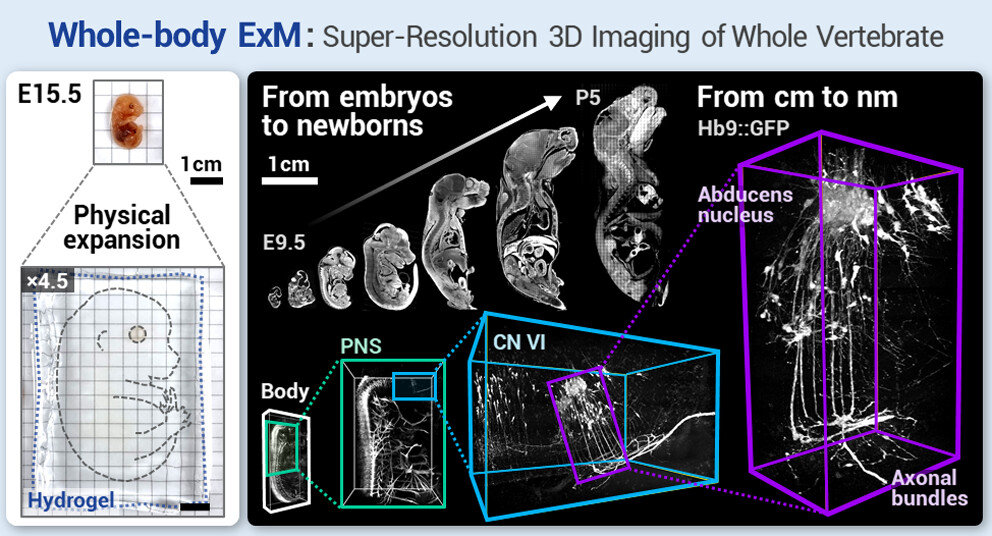
概要
本研究では、拡張顕微鏡(Expansion Microscopy, ExM) を応用し、マウス胎児全体をナノスケールでイメージング する技術「whole-body ExM」を開発した。本手法では酵素消化を繰り返すサイクル消化法 を用いることで、従来困難とされていた骨や軟骨を含むマウス胎児の均一な膨張 を実現。最大4倍の膨張 により、マウス胎児および新生児の超解像3Dイメージング を可能にした。さらに、蛍光タンパク質(FP)シグナルを保持することができるため、神経系構造の詳細な観察 も可能となる。本手法は、脊椎動物の分子レベルの研究を加速する可能性がある。
背景
- マウス胎児のナノスケールイメージング は、発生生物学や神経科学において極めて重要。
- 既存技術(組織透明化、電子顕微鏡、CTなど)は全身イメージング には適しているが、100 nm未満の解像度 での観察が困難。
- 拡張顕微鏡(ExM) は60 nmの分解能を持つが、骨を含む脊椎動物全体の拡張 は未解決の課題であった。
方法
- サイクル消化法(proteinase Kとコラゲナーゼの交互適用)により、骨・軟骨を含むマウス胎児全体の均一な拡張 を実現。
- 発生段階ごとに消化サイクル数 を最適化し、E9.5〜E18.5および新生児の拡張を可能にした。
- 蛍光タンパク質(FP)シグナル保持 により、神経系や組織構造を鮮明に可視化。
- 抗体染色や全身免疫染色 との適合性を検証。
- 画像解析 により、拡張後の構造の均一性・等方性(isotropy)を評価。
結果
- サイクル消化法により、4倍の均一な膨張が可能(E9.5〜新生児まで適用可能)。
- 蛍光タンパク質(FP)のシグナルを保持 し、神経系の詳細な観察が可能。
- 全身免疫染色との互換性 を示し、多様なタンパク質の可視化が可能。
- ナノスケールの等方性検証(誤差3.2%) により、均一な拡張を確認。
- 運動神経や迷走神経の全身マッピング を実施し、発生過程における詳細な構造を解明。
考察
- 既存技術では困難だった全身超解像イメージング を実現。
- 脊椎動物の全身イメージング技術として、ExMの適用範囲を大幅に拡大。
- 神経発生学・再生医療・疾患研究 への応用が期待される。
- 他の組織透明化技術やExMの多重拡張技術との統合 も今後の課題。
従来研究との新規性
- ExMを脊椎動物全体に適用し、骨を含む胎児の均一な拡張を実現(初の試み)。
- サイクル消化法の開発により、発生段階ごとの適用を可能に。
- 蛍光タンパク質シグナル保持により、詳細な神経マッピングを実現。
限界
- 新生児以降の大きな個体への適用(膨張後の物理的強度の低下)。
- 拡張後の蛍光シグナルの減衰(一部抗体の非特異的結合が観察される)。
- 超高倍率顕微鏡の導入により、さらなる解像度向上が可能だが、撮影時間が長い。
潜在的な応用
- 発生生物学: 胚発生過程の詳細な解析
- 神経科学: 迷走神経・脊髄神経の全身ネットワーク解析
- 疾患研究: 神経変性疾患(ALS, CMT, ヒルシュスプルング病など)の発症機序解析
- 再生医療: 神経再生・移植研究への応用
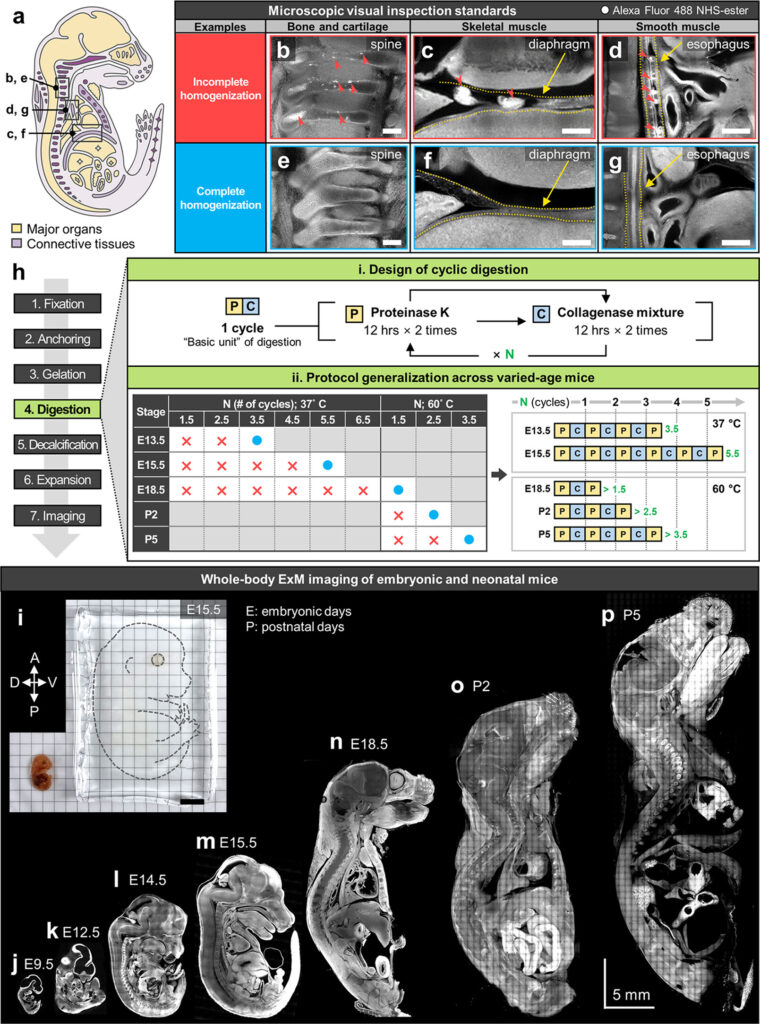
Figure 1: Whole-Body ExMプロトコルの開発と一般化
(a) E15.5マウス胎児の解剖学的特徴を示す模式図
- 主要な臓器(黄色) と 結合組織(紫色) を示す。
(b–d) 不完全な消化による組織の変形
- (b) 脊椎, (c) 横隔膜, (d) 食道 の拡張後の変形を観察。
- 赤い矢印 は、消化の不完全さに起因する局所的な組織の歪みを示す。
(e–g) 完全に消化され、均一に拡張されたマウス胎児スライス
- (e) 脊椎, (f) 横隔膜, (g) 食道 の均一な拡張を示す。
(h) Whole-Body ExMのワークフローとサイクル消化の概念
- i. サイクル消化の設計: プロテイナーゼKとコラゲナーゼを交互に適用。
- ii. 異なる発生段階のマウスに適用可能なプロトコルの一般化。
(i) E15.5マウス胎児のWhole-Body ExM前後の写真
- 左: 未拡張の胎児半分
- 右: 4.5倍に拡張された胎児半分
(j–p) さまざまな発生段階のマウス胎児および新生児の代表的な共焦点画像
- (j) E9.5, (k) E12.5, (l) E14.5, (m) 500 µm厚E15.5, (n) 500 µm厚E18.5, (o) 1 mm厚P2, (p) 500 µm厚P5 のマウスサンプルを観察。
- 染色: (b–g, j, k, m, n, p) Alexa Fluor 488 NHSエステル, (l) ATTO 647N NHSエステル, (o) CF568 NHSエステル。
要点まとめ
- サイクル消化法により、骨を含む組織の均一な拡張が可能に。
- 胎児の発生段階に応じて適切な消化サイクルを設定し、全身拡張を実現。
- 拡張後も組織の形態を保持し、超解像イメージングが可能。
