ChemMedChem. 2024 Dec 23:e202400851. doi: 10.1002/cmdc.202400851. Online ahead of print.
Thiazole-Based IL-17 Inhibitors Discovered by Scaffold Morphing (足場モーフィングによって発見されたチアゾール系IL-17阻害剤)
Juraj Velcicky 1, Estelle Ngo 1, Matthias R Bauer 1, Arndt Meyer 1, Achim Schlapbach 1, Sophie Racine 1, David Orain 1, Daniel Pflieger 1, Sylvie Teixeira-Fouchard 1, Celine Dubois 1, Alban Goetz 1, Roland Steiner 1, Marco Palmieri 1, Alex Bussenault 1, Rowan Stringer 1, Patrice Larger 1, Simone Riek 1, Patrick Schmutz 1, Sylvie Lehmann 1, Clemens Scheufler 1, Jean-Michel Rondeau 1, Christoph Burkhart 1, Thomas Knoepfel 1, Nina Gommermann 1
Novartis Biomedical Research, Novartis Campus, 4056, Basel, Switzerland.
ノバルティスバイオメディカル研究所(Novartis Institute for BioMedical Research)は、スイスのノバルティス社が運営する創薬研究部門である。
Point
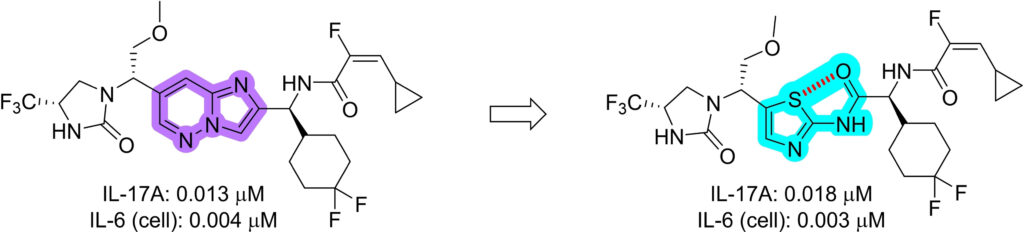
IL-17Aはセクキヌマブのような抗体薬が市販されているが、この論文では低分子阻害剤を紹介している。IL-17阻害剤のSAR 平面性を保った構造変換を行い、イミダゾピリダジン構造をチアゾールアミドに置き換えることで、分子が平面共役構造を保つようにデザインされている。この変換では、硫黄と酸素間の相互作用を利用して、イミダゾピリダジン構造が持っていた平面構造を模倣している。X線構造解析によりこの新しいチアゾールアミドシリーズがIL-17との結合において高い効力を持つことが確認されている。
Abstract
The pro-inflammatory cytokine interleukin-17A (IL-17) plays an important role in the body’s defense against bacterial and fungal infections. However, overexpression of IL-17 has been associated with several diseases, including rheumatoid arthritis, asthma, psoriasis, and even cancer. The role of IL-17 in psoriasis has been confirmed by clinical use of IL-17 antibodies, e. g. secukinumab (Cosentyx®). Ongoing research is focused on discovering low molecular weight IL-17 inhibitors. In this publication, we present thiazole-based IL-17 inhibitors discovered through a scaffold-morphing strategy. This strategy involved ring-opening of a known scaffold and utilization of a chalcogen interaction between thiazole-sulfur and central amide-oxygen to maintain the coplanar conformation found in the parent compound. The new scaffold enabled the generation of highly potent compounds with good overall profile. The optimized compounds 11 and 15 demonstrated good exposure in rats after oral dosing. Importantly, compound 11 exhibited no adverse effects in a rat tolerability study after a four-day administration of up to 300 mg/kg/day.
炎症促進性サイトカインであるインターロイキン-17A(IL-17)は、細菌や真菌感染に対する生体防御において重要な役割を果たしている。しかし、IL-17の過剰発現は、関節リウマチ、喘息、乾癬、さらには癌を含むいくつかの疾患と関連している。乾癬におけるIL-17の役割は、IL-17抗体、例えばセクキヌマブ(Cosentyx®)の臨床使用により確認されている。現在進行中の研究では、低分子のIL-17阻害剤の発見に焦点が当てられています。本論文では、足場モーフィング戦略により発見されたチアゾール系IL-17阻害剤を紹介する。この戦略では、既知の足場を開環し、チアゾール硫黄と中心のアミド酸素間のカルコゲン相互作用を利用して、親化合物で見られる共平面構造を維持した。この新しい骨格により、全体的なプロファイルが良好で、非常に強力な化合物の生成が可能になりました。最適化された化合物11と15は、経口投与後のラットにおいて良好な曝露を示した。重要なのは、化合物11が最大300mg/kg/日の4日間投与後のラット耐容性試験において、有害な影響を示さなかった。
背景
- IL-17Aの役割:
IL-17Aは主にTh17細胞から分泌され、免疫応答において重要な役割を果たすサイトカインであるが、その過剰な活性化は関節リウマチ、喘息、乾癬、さらにはがんと関連している。IL-17を標的とする抗体(例: Secukinumab)は既に臨床で使用されており、IL-17阻害の有効性が示されている。 - 低分子阻害剤の必要性:
モノクローナル抗体のような生物学的製剤には製造コストや投与方法の制限があるため、低分子化合物の開発が進められている。
方法
- 足場モルフィング:
従来のIL-17阻害剤(例: Imidazopyridazine系)の中心二環構造を開環し、平面構造を維持するチアゾールアミドを新たな足場として採用した。この設計において、チアゾール硫黄と中央アミド酸素のカルコゲン相互作用が重要とされた。 - 合成プロセス:
多段階の化学反応を経て最適化された誘導体が合成された(詳細は図や化学式に基づいて説明されている)。
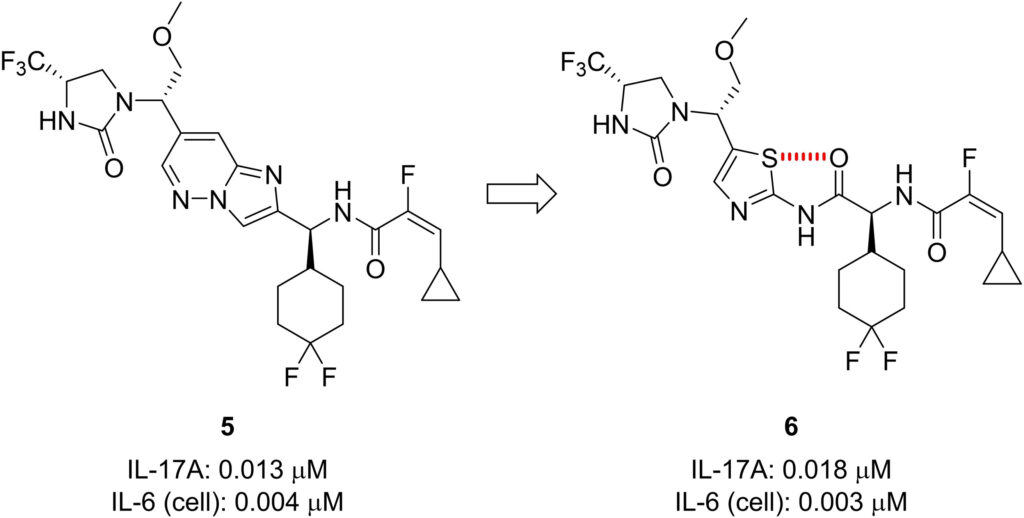
図2では、既存のIL-17阻害剤の中心二環構造を開環して、新しいチアゾールアミド足場に変換するプロセスが示されている。このデザインは、以下のポイントに基づいている。
- 二環構造の開環:
- 元の二環式イミダゾピリダジン骨格(従来の足場)を分解して平面構造を維持しつつ、中心部分を新しい構造に置き換える。
- 具体的には、中央部分を「アシル2-アミノチアゾール」に変換しています。
- カルコゲン相互作用の利用:
- 新しい足場では、チアゾール内の**硫黄原子(S)**と隣接するアミド酸素(O)との間にカルコゲン相互作用(S···O)が形成されます。
- この相互作用により、分子が目標とする平面構造を維持することが可能になります(赤い点線で示されています)。
- 重要な水素結合の維持:
- 新しい足場では、IL-17Aとの結合に必要な4つの水素結合が維持されます。これにより、標的タンパク質(IL-17Aホモ二量体)との結合が強化されます。
- 全体のコンセプト:
- 新しい設計は、従来の化合物の課題(毒性や低い溶解性など)を克服しつつ、阻害活性を向上させることを目的としています。
結果
- 化合物11の特性:
化合物11は、優れた経口吸収性、低い毒性、そして高い薬物動態安定性を示した。具体的には、300 mg/kg/日の経口投与を4日間行ったラット試験で、毒性所見が認められなかった。 - X線結晶構造解析:
IL-17Aホモ二量体との結合様式を解析したところ、カルコゲン相互作用を介して平面構造が維持され、重要な水素結合(Leu120、Trp90との相互作用)が確認された。 - 比較試験:
化合物11は他の誘導体と比較して、特に薬物動態の面で優れた結果を示した。化合物15も好ましい特性を持っていたが、化合物11の安定性には及ばなかった。
考察
- 設計の妥当性:
チアゾールアミドの導入により、IL-17A阻害剤としての活性が維持され、さらに物理化学特性の改善が見られた。特にカルコゲン相互作用が設計の鍵となった。 - 毒性の軽減:
これまでの足場(例: LY3509754)が毒性のために中止されたことを踏まえ、本研究では全く異なる足場を設計することで毒性の低減が図られた。
従来の研究との新規性
- 足場モルフィングによる全く新しいアプローチ。
- チアゾールアミド構造がIL-17Aとの結合を強化。
- X線解析を通じて、設計仮説の分子レベルでの確認。
潜在的応用
- 医療分野:
関節リウマチ、乾癬、その他の自己免疫疾患の治療薬として期待される。 - 創薬分野:
他のサイトカインを標的とした薬剤設計にも応用可能。



